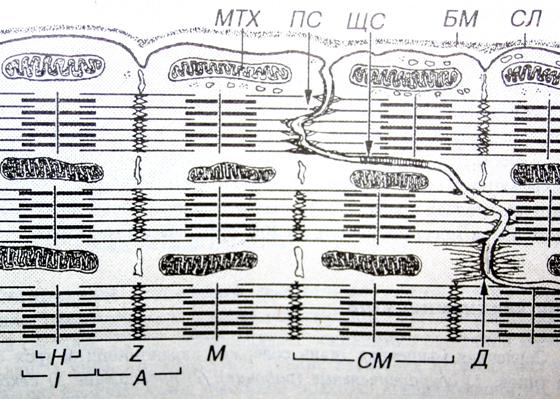
Механизмы миофибриллярной гипертрофии скелетных мышц человека
В статье рассмотрены механизмы миофибриллярной гипертрофии скелетных мышц человека с позиций ряда медико-биологических дисциплин: анатомии, гистологии, цитологии, биохимии, физиологии и спортивной медицины. В публикации анализируются различные гипотезы, объясняющие механизмы повышенного синтеза белка в мышцах под воздействием тренировки силовой направленности. В настоящее время наиболее распространена гипотеза механического повреждения мышечных волокон.
Самсонова А.В. Механизмы миофибриллярной гипертрофии скелетных мышц человека //Мат. 1 Всерос. Конф. С межд. Участием «Совершенствование учебного процесса в условиях современного вуза».- Белгород: БегГУ, 2012.- С. 388-395
Самсонова А.В.
МЕХАНИЗМЫ ГИПЕРТРОФИИ СКЕЛЕТНЫХ МЫШЦ ЧЕЛОВЕКА
ВВЕДЕНИЕ
Миофибриллярная гипертрофия – адаптация скелетных мышц человека к силовым нагрузкам при направленности тренировочного процесса на увеличение их объема или силы. Установлено, что при этом типе гипертрофии возрастает количество и объем миофибрилл – основных элементов мышечного волокна [2, 10, 22].
Целью исследования являлась разработка концепции, описывающей механизмы миофибриллярной гипертрофии скелетных мышц человека под воздействием нагрузок силовой направленности.
РЕЗУЛЬТАТЫ
В настоящее время существует несколько гипотез, объясняющих повышенный синтез белка в скелетных мышцах человека.
В основе первой гипотезы – энергетической [2, 10, 22] – лежит предположение о том, что нарушение равновесия между потреблением и восстановлением основной энергетической «валюты» – АТФ – стимулирует процессы, протекающие в мышцах, в результате чего происходит их гипертрофия. Известно, что содержание в мышце АТФ ограничено. При проведении интенсивных силовых тренировок в мышцах возникает недостаток АТФ, что является для организма серьезным предупреждающим сигналом. Недостаток АТФ неблагоприятно сказывается на метаболизме белка. Следует отметить, что в результате интенсивных силовых тренировок происходит также большое разрушение белков мышц. Расходуются не только миофибриллярные белки, но и ферменты и гормоны (функциональные белки), которые играют важную роль в сокращении мышц. Известно, что белки состоят из аминокислот. Основой аминокислот является азот. Установлено, что силовые тренировки приводят к выделению большого количества азота в виде продуктов распада мышечных белков (мочевина). Во время напряженных силовых тренировок и непосредственно после них распад белка значительно превосходит его восстановление. По мнению [10], это связано, в первую очередь, с нехваткой АТФ. Таким образом, равновесие между постоянно протекающими процессами распада и восстановления, которое наблюдается в нормальных условиях, серьезно нарушается. В последующих фазах восстановление белковых структур с помощью пищи, богатой протеинами, осуществляется настолько интенсивно, что их количество превышает исходный уровень за счет явления суперкомпенсации. Вследствие этого увеличивается площадь поперечного сечения миофибрилл. Повторные интенсивные тренировки воздействуют уже на большую площадь миофибрилл. Таким образом, интенсивные силовые тренировки становятся менее опасными для организма. Помимо увеличения площади поперечного сечения миофибрилл и их количества, в мышечных волокнах происходит заметное увеличение запасов фосфатных соединений, богатых энергией. Таким образом, организм приспосабливается к нагрузке.
Более подробно о механизмах гипертрофии мышц Вы можете прочесть в моей книге «Гипертрофия скелетных мышц человека«
В основе второй гипотезы [8, 9] лежит предположение о том, что пусковым стимулом синтеза белка в мышцах является их ацидоз[1], вызванный накоплением в мышцах кислых продуктов метаболизма (ионов водорода), а также увеличение содержания в мышечных волокнах креатина.
Схема повышенного синтеза белка выглядит следующим образом. В ходе выполнения силовых упражнений с большими отягощениями (до 80% от максимума) энергия АТФ тратится на выполнение механической работы. Ресинтез АТФ начинается благодаря запасам креатинфосфата в мышечном волокне. В результате чего в мышечном волокне появляется креатин. Накопление креатина в саркоплазматическом пространстве служит мощным эндогенным стимулом, возбуждающим белковый синтез в скелетных мышцах. Показано, что между содержанием сократительных белков и содержанием креатина имеется строгое соответствие. Креатин, видимо, воздействует на синтез иРНК (информационной РНК), т.е. на процессы транскрипции в ядрах мышечных волокон.
Креатин активизирует деятельность всех метаболических путей, связанных с образованием АТФ (гликолиз в саркоплазме, аэробное окисление в митохондриях). Так как мощность гликолиза меньше скорости потребления АТФ, а мощность аэробного окисления еще ниже, чем гликолиза, в клетке начинают накапливаться ионы водорода, лактат и АДФ. Повышение концентрации ионов водорода вызывает лабилизацию мембран (увеличение размеров пор в мембранах, что ведет к облегчению проникновения гормонов в клетку), активизирует действие ферментов, облегчает доступ гормонов к наследственной информации, к молекулам ДНК. В ответ на одновременное повышение концентрации креатина и ионов водорода в ядрах клетки интенсивнее образуется РНК.
В основе третьей гипотезы лежит предположение, что пусковым стимулом для возрастания синтеза белка в мышцах является гипоксия[2]. Такое предположение связано с тем, что при выполнении упражнений силовой направленности при напряжении мышцы более 60% от максимума, капилляры и артериолы мышцы сдавливаются, и кровь к сокращающимся мышцам не поступает [22].
Гипоксия, развивающаяся в мышцах в процессе нагрузки, ведет к накоплению кислых метаболитов и закислению саркоплазмы. Калиемия, вызывающая сужение кровеносных сосудов, усиливает состояние гипоксии. Энергетические ресурсы ткани истощаются. Изменение энергетического метаболизма проявляется в нарушении транспорта ионов через мембраны клеток, повышении концентрации кальция и активации протеолиза[3]. В первую очередь, активируются калпаины – нелизосомальные протеазы, которые играют важную роль в запуске расщепления белков скелетных мышц, воспалительных изменениях и процессе регенерации. После окончания выполнения физических упражнений за гипоксией следует реперфузия[4]. Доказано, что интенсивные физические нагрузки вызывают сильную метаболическую гипоксию мышц, последствия которой после прекращения нагрузки оказываются сходными с последствиями реперфузии при ишемии. Приток кислорода в мышцы остается на высоком уровне, хотя метаболический запрос ткани в отношении кислорода снижается. Это вызывает активацию процессов перекисного окисления липидов (ПОЛ), что нарушает целостность сарколеммы мышечного волокна, повреждение и деградацию его сократительных белков, а также белков цитоскелета [11]. Одновременно с этим в мышечном волокне развиваются воспалительные процессы, что выражается в повышении содержания лейкоцитов в скелетных мышцах через 24 часа после тренировки. Каскад процессов, происходящих в мышце после тренировки, приводит к появлению запаздывающих болевых ощущений и ухудшению функционального состояния мышцы, что выражается в уменьшении уровня максимальной силы. Затем в поврежденных мышечных волокнах активируются клетки-сателлиты, которые активно участвуют в регенерации мышцы и восстановлении ее функциональной активности [4, 5].
В основе четвертой гипотезы, которая получила в настоящее время широкое распространение, лежит предположение о том, что пусковым стимулом для возрастания синтеза белка в мышцах является механическое повреждение мышечных волокон и миофибрилл, после которого следует их регенерация.
Доказано, что после больших физических нагрузок происходит повреждение мышечных волокон [12, 15, 3]. Д.Дж. Нейман с соавт. [20] показали, что сразу после физических упражнений 16% мышечных волокон имели легкие повреждения, 16% – более сильные и 8% — очень сильные. Кроме того, эти авторы утверждали, что повреждения, замеченные немедленно после выполнения упражнения, были предшественниками более сильных повреждений, которые отмечались в последующих биопсиях. Ж.Фрайден с соавт. [13] показали, что через час после выполнения эксцентрических упражнений у человека в 32% мышечных волокон были обнаружены повреждения, а через три дня повреждения были обнаружены в 52% мышечных волокон. М.Джибала с соавт. [15] установили, что даже однократная высокоинтенсивная силовая тренировка приводит к повреждению большого количества мышечных волокон (от 30 до 80%). При этом более сильные повреждения обнаруживаются в волокнах II типа по сравнению с волокнами I типа [13]. Установлено также, что волокна II типа повреждаются в первую очередь [16].
Из компонентов мышечного волокна сильные повреждения наблюдаются в сарколемме, саркоплазматическом ретикулуме, миофибриллах, цитоскелете. Наиболее подверженными разрушению оказываются Z-диски мышечного волокна [12, 14, 15]. Если повреждается сарколемма мышечного волокна, в крови появляются ферменты, содержащиеся в саркоплазме. Очень часто в крови обнаруживается фермент креатинкиназа, который участвует в креатинфосфатном пути ресинтеза АТФ. Доказано, что содержание в крови ферментов после значительных нагрузок силовой направленности может увеличиваться в 100 раз [3]. Показано, что повреждение мышечных волокон различных типов можно диагностировать посредством определения в сыворотке крови легкой и тяжелой изоформ миозина. При изучении различной степени повреждения мышцы установлено, что при самых легких повреждениях мышечных волокон уровень легкой изоформы миозина увеличивается с 625 мг/л до 2880 мг/л, то есть более чем в 4 раза [16]. Появление в крови легкой изоформы миозина свидетельствует о повреждении мышечных волокон II типа. Повреждение мышечных волокон сопровождается запаздывающими болевыми ощущениями (DOMS). Повреждение мышечных волокон и миофибрилл запускает процессы регенерации мышечной ткани (рис.1).
Рис. 1. Схематическое повреждение мышечного волокна [19]. Обозначения: А – напряжение мышцы ведет к повышению концентрации ионов кальция (черные кружки); В – повышение концентрации ионов кальция приводит к активации калпаинов и избирательному повреждению элементов цитоскелета; С – последующая активность мышцы повреждает цитоскелет.
Если мышечное волокно было разорвано или повреждено, в поврежденном участке образуется некротическая зона. При этом на некотором расстоянии от места травмы возникает полное разрушение сарколеммы, саркоплазмы и органелл, хотя за пределами этой зоны волокно сохраняет свою жизнеспособность. Считается, что этот процесс инициируется увеличенным количеством внутриклеточного кальция (Са 2+ ), который поступает в саркоплазму мышечного волокна из поврежденного саркоплазматического ретикулума. Ионы кальция активируют ферменты – протеазы, которые расщепляют белки в миофибриллах. В первую очередь, активируются калпаины – протеолитические ферменты, которые воздействуют на белки цитоскелета [14, 16]. Именно белки цитоскелета разрушаются в первую очередь [19, 14]. Появление в волокне обрывков белковых молекул активирует лизосомы, переваривающие с помощью содержащихся в них ферментов белковые структуры, которые необходимо уничтожить. Если лизосомы не справляются с объемом работы, то через сутки активируются более мощные чистильщики – фагоциты. Фагоциты – клетки, находящиеся в крови и тканевой жидкости. Основная их задача – уничтожение поврежденных тканей и чужеродных микроорганизмов. Фагоциты проникают в волокно, потребляют его содержимое и выводят остатки. Именно продукты жизнедеятельности фагоцитов вызывают воспалительные процессы в мышцах через сутки после тренировки. В это же время в мышечном волокне начинается процесс его «ремонта». С гистологической точки зрения, при регенерации возможно не только восстановление целостности поврежденных мышечных волокон, но и возникновение новых мышечных волокон [1, 3]. Регенерация идет тем интенсивнее, чем больше освобождается из-под базальной мембраны клеток-сателлитов.
Иногда сильные повреждения обнаруживаются в миофибриллах, хотя внешне мышечное волокно сохраняет свою целостность. Некоторые саркомеры могут быть более растянутыми по сравнению с другими. Это означает, что поврежден цитоскелет мышечного волокна, то есть продольные филаменты, связывающие соседние саркомеры в одной миофибрилле, а также поперечные филаменты, связывающие соседние миофибриллы между собой и с сарколеммой. Повреждение цитоскелета неизбежно приводит к незначительным повреждениям сарколеммы и как следствие – активации деятельности клеток-сателлитов, которые в мышечном волокне располагаются между сарколеммой и базальной мембранной.
Многочисленными исследованиями доказано, что в результате выполнения силовых упражнений, в первую очередь, повреждаются Z-диски, соединяющие саркомеры друг с другом в миофибрилле. Напомним, что к Z-дискам прикрепляются тонкие филаменты. Считается, что Z-диски являются «слабым звеном» миофибриллы. При этом возможен как полный разрыв миофибрилл в области Z-дисков так и растягивание Z-дисков с сохранением целостности миофибриллы (рис. 2).
ВЫВОДЫ
БИБЛИОГРАФИЧЕСКИЙ СПИСОК
[1] Ацидоз – закисление внуренней среды организма, связано с накоплением в тканях кислых продуктов обмена веществ. При напряженной мышечной работе ацидоз приводит к развитию утомления.
[3] Протеолиз – распад белков, приводящий к образованию аминокислот.
[4] Реперфузия – возобновление притока кислорода к тканям.
Что является частью миофибриллы
Введение
В современной медицине все больший интерес вызывают вопросы лечения и профилактики заболеваний сердечно-сосудистой системы, возникновение которых в значительной мере связано с нарушением структуры и функций сердечной мышечной ткани (атеросклероз, инфаркт миокарда, гипертензия, астма и др.). В связи с необходимостью более глубокого изучения этиологии и патогенеза заболеваний сердечно-сосудистой системы, познания механизмов, лежащих в основе этих состояний, возрастает интерес к фундаментальным исследованиям структурно-функциональных особенностей сердечной мышечной ткани.
1 Общая характеристика сердечной мышечной ткани
Стенка сердца состоит из трех оболочек:
В организме человека все мышечные ткани, в том числе и сердечная мышечная ткань, специализированы на функции сокращения и развиваются на общей основе: гипертрофии и видоизменении сократимой механической актин-миозиновой системы.
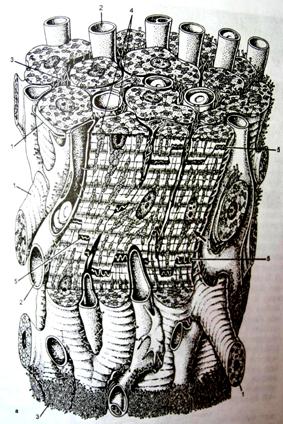
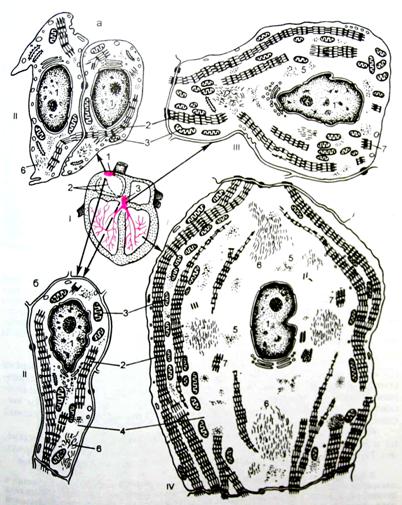
Сердечная мышечная ткань относится к поперечнополосатой мышечной ткани целомического типа, встречается только в мышечной оболочке сердца (миокарде) и устьях связанных с ним крупных сосудов; образована структурными элементами (клетками, волокнами), которые имеют поперечную исчерченность вследствие особого упорядоченного взаиморасположения в них актиновых и миозиновых миофиламентов и обладает спонтанными (непроизвольными) ритмическими сокращениями (рис. 1).
Основным функциональным свойством сердечной мышечной ткани является способность к спонтанным ритмическим сокращениям, на активность которых влияют гормоны и нервная система (симпатическая и парасимпатическая).
Для понимания структурно-функциональных особенностей сердечной мышечной ткани рассмотрим процессы ее формирования в период развития сердца и кардиомиогенеза.
2 Развитие сердца и кардиомиогенез
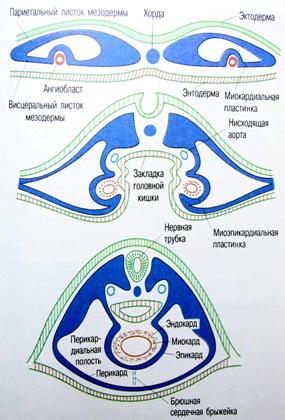
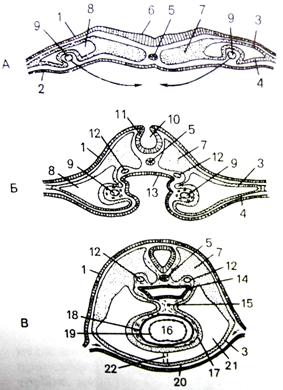
Закладка сердца человека происходит в начале 3-й недели развития (у эмбриона длиной 1,5 мм) и представлена парным скоплением мезенхимных клеток в задней части головного отдела эмбрионального щитка под висцеральным листком мезодермы (рис. 2, 3). С течением времени эти скопления превращаются в две удлиненные трубки, вдающиеся вместе с висцеральным листком мезодермы в целомическую полость тела, и выстилаются эндотелием. Позднее мезенхимные трубки сливаются и из их стенок образуется эндокард.
Рис. 3. Развитие сердца человека
Перикард формируется из париетального листка мезодермы.
Широкое пространство между эндотелиальными трубочками и миокардиальной пластинкой заполняется эндокардиальным гелем.
По мнению А.Г. Кнорре слой образующегося эпикарда (его мезотелиальное покрытие) нарастает на зачаток миокарда позднее, со стороны венозного синуса. Поэтому первичную закладку сердца предлагается называть не миоэпикардиальной пластинкой, а миокардиальной.
Клетки зачатка миокарда (миокардиальная пластинка), т.е. кардиомиобласты, производят процесс деления и на 2-м месяце эмбрионального развития в них появляются миофибриллы с поперечной исчерченностью. Z-полоски появляются одновременно с саркотубулярной сетью и поперечными инвагинациями клеточной мембраны (Т-системы). На плазмолеммах контактирующих миобластов образуются десмосомы. Формирующиеся миофибриллы прикрепляются к плазмолеммам, где позднее образуются вставочные диски.
В конце 2-го месяца начинает формироваться проводящая система сердца, завершение образования всех отделов которой завершается к 4-му месяцу. Развитие мышечной ткани левого желудочка происходит быстрее, чем правого.
Опорный скелет сердца образован фиброзными кольцами между предсердиями и желудочками и плотной соединительной тканью в устьях крупных сосудов. Кроме плотных пучков коллагеновых волокон, в состав опорного скелета сердца входят эластические волокна, а иногда встречаются хрящевые пластинки.
В процессе развития сердце человека увеличивается в объеме в 16 раз в сравнении с сердцем новорожденного, при этом в 15 раз возрастает объем кардиомиоцитов.
Таким образом, рост миокарда происходит из-за полиплоидизации ядер кардиомиоцитов и гипертрофии, которая свойственна внутриклеточной регенерации, т.е. умножением числа внутриклеточных структур и увеличением массы гиалоплазмы. Полиплоидизация и гипертрофия обеспечивают увеличение миокарда при его развитии, а также осуществляют компенсационный рост ответ на повышенную нагрузку на сердце, когда может происходить небольшой всплеск митотической активности, но часто без цитотомии.
В процессе развития сердечной мышечной ткани происходит инверсия митотического индекса: на ранних этапах развития максимальная пролиферативная активность наблюдается в желудочках, а позднее более интенсивно митозируют миоциты предсердий.
Итак, кардиомиоциты представляют собой некамбиальную, медленно растущую популяцию, не имеющую сателлитов.
2.1 Строение внутренней оболочки сердца эндокарда
Питание эндокарда производится в основном диффузно из-за наличия крови, находящейся в сердечных камерах. Кровеносные сосуды имеются только в наружном соединительнотканном слое эндокарда.
2.1.1 Клапаны сердца
Левый предсердно-желудочковый клапан появляется в виде эндокардиального валика, в который к 2,5 месяцам врастает соединительная ткань из эпикарда. На 4-м месяце из эпикарда в створку клапана врастает пучок коллагеновых волокон, образующий позже фиброзную пластинку. Правый предсердно-желудочковый клапан закладывается как мышечно-эндокардиальный валик. С 3-го месяца эмбриогенеза мышечная ткань правого атриовентрикулярного клапана уступает место соединительной ткани, врастающей со стороны миокарда и эпикарда. У взрослого человека мышечная ткань сохраняется в виде рудимента только с предсердной стороны в основании клапана. Таким образом, предсердно-желудочковые клапаны являются производными как эндокарда, так и соединительной ткани миокарда и эпикарда.
На границе между восходящей частью дуги аорты и левым желудочком сердца локализуются аортальные клапаны, которые по своему строению имеют много общего с предсердно-желудочковыми клапанами и клапанами легочной артерии.
2.2 Строение средней оболочки сердца миокарда
Различают два типа кардиомиоцитов:
2.2.1 Сердечные миоциты желудочков и предсердий
Рис. 4. Строение кардиомиоцита сердца.
Т-каналы желудочковых миоцитов имеют характер глубоких поперечных складок на уровне линий Z, их продольных ветвей и анастомозов вблизи дисков А. Объем Т-системы в желудочковых миоцитах составляет 27-36% от объема цитоплазмы. По каналам данной системы у кардиомиоцитов не только распространяется импульс, но и поступают метаболиты в клетку.
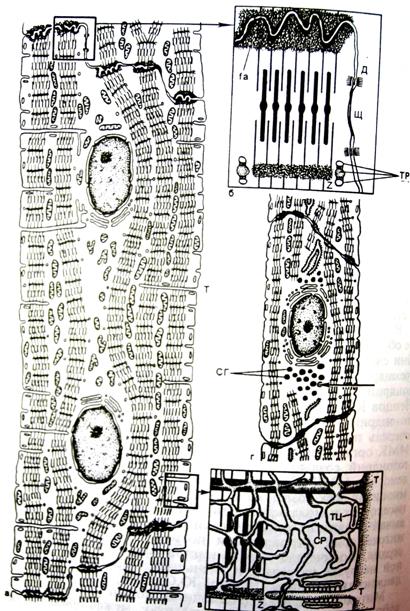
Специализированными структурами кардиомиоцитов являются «вставочные диски», которые представляют собой комплекс, состоящий из промежуточных соединений (fascia adherens), нексусов (щелевые контакты) и десмосом (рис. 5, 6). Вставочные диски всегда находятся на уровне линий Z и содержат плотный материал, в котором много липидов и ряд белков, в том числе α-актинин, виментин, винкулин, десмин, спектрин, коннектин и др.
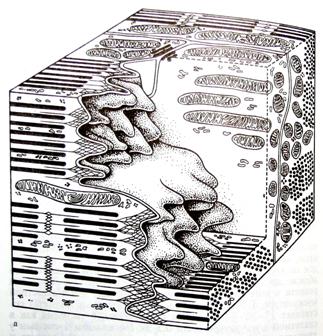
Рис. 5. «Вставочные диски» кардиомиоцитов
Объемная модель фрагментов двух кардиомиоцитов на уровне вставочного диска. Видны пальцевидные выросты клеток, которые на срезе имитируют рисунок «вставочного диска»
Рис. 6. Ультраструктурная организация области «вставочного диска» кардиомиоцитов
Клеточные соединения в виде десмосом имеют характерное строение, а нексусы в основном располагаются вдоль продольной оси клетки. В этих образованиях сближаются мембраны контактирующих клеток, образуя многочисленные коннексоны, при этом через гидрофильный канал распространяется нервный импульс и происходит обмен метаболитами между соседними миоцитами. Промежуточные соединения, или полоски слипания, представляют собой уплотненные участки плазмоллем контактирующих клеток и связывают конечные саркомеры соседних миоцитов. Вставочные диски соединяют друг с другом продольно лежащие миоциты с образованием тяжей или функциональных волокон. Часто плотные вставочные диски имеют ступенчатый вид.
Рабочие миоциты предсердий в отличие от желудочковых содержат секреторные гранулы и имеют способность к митозу. Данные миоциты мельче желудочковых и часто с отростками. Миофибриллярных элементов в них меньше на 40%, и реже наблюдаются лестничные структуры во вставочных дисках. Гранулярный эндоплазматический ретикулум и аппарат (комплекс) Гольджи развиты в этих клетках сильнее, чем в желудочковых миоцитах. Характерно, что Т-система в рабочих миоцитах предсердий почти не развита и если присутствуют, то каналы располагаются вдоль, а не перпендикулярно продольной оси клетки.
2.2.2 Сердечные миоциты проводящей системы сердца
Миоциты проводящей системы сердца (рис. 7). К проводящей системе сердца (systema conducens cardiacum) относятся мышечные клетки, формирующие и проводящие импульсы к сократительным клеткам сердца. В состав проводящей системы входят синусно-предсердный и предсердно-желудочковый узлы, предсердно-желудочковый пучок (пучок Гиса), его ножки и концевые разветвления ножек, образованные клетками Пуркинье. В сердце человека клетки проводящей системы сильно отличаются по размерам и структуре от рабочих миоцитов. Различают три типа мышечных клеток, которые в разных соотношениях находятся в соответствующих отделах данной системы.
Рис. 7. Кардиомиоциты проводящей системы сердца
Другим типом клеток синусного узла, находящегося по его периферии, является переходный, или латентный тип. В таких клетках больше миофибрилл и нексусов, а в некоторых из них есть Т-каналы. Данные клетки проводят импульс из синусного узла к другим клеткам предсердия, а именно от Р-клеток к клеткам предсердно-желудочкового пучка и рабочему миокарду.
Предсердно-желудочковый узел имеет клетки, схожие с миоцитами синусного узла. Оба узла сильно иннервированы с преобладание адренергических терминалей. Каждый миоцит имеет и афферентную, и эфферентную иннервации.
Предсердно-желудочковый пучок (пучок Гиса) представляет прямое продолжение предсердно-желудочкового узла и покрыт «чехлом» из плотной соединительной ткани. Ножки пучка разветвляются под эндокардом, а также по толщине миокарда желудочков и проникают в сосочковые мышцы.
В проводящей системе сердца преобладают энзимы, принимающие участие в анаэробном гликолизе (фосфорилаза, дегидрогеназа молочной кислоты). В проводящих волокнах уровень калия ниже, а кальция и натрия выше в сравнении с сократительными кардиомиоцитами.
2.3 Строение наружной оболочки сердца эпикарда и перикарда
Наружная оболочка сердца, или эпикард (epicardium), представляет висцеральный листок перикарда (pericardium). Эпикард образован тонкой пластинкой соединительной ткани, плотно срастающейся с миокардом. Свободная поверхность ее покрыта мезотелием. В основе эпикарда различают поверхностный слой коллагеновых волокон, слой эластических волокон, глубокий слой коллагеновых волокон и глубокий коллагеново-эластический слой, составляющей до 50% всей толщины эпикарда.
В перикарде соединительнотканная основа развита сильнее, чем в эпикарде. Здесь много эластических волокон, особенно в глубоком его слое. Поверхность перикарда, обращенная к перикардиальной полости, также покрыта мезотелием. Эпикард и париетальный листок перикарда имеют многочисленные нервные окончания в основном свободного типа.
3. Васкуляризация сердца
Венечные (коронарные) артерии имеют плотный эластический каркас, в котором выделяются внутренняя и наружная эластические мембраны. Гладкие мышечные клетки в артериях обнаруживаются в виде продольных пучков во внутренней и наружной оболочках.
В основании клапанов сердца кровеносные сосуды в месте прикрепления створок разветвляются на капилляры, откуда кровь собирается в коронарные вены, впадающие в правое предсердие или венозный синус. В эпикарде и перикарде также находятся сплетения сосудов микроциркуляторного русла. Проводящая система сердца, особенно ее узлы, обильно снабжена кровеносными сосудами.
Кровоснабжение сердечной мышечной ткани чрезвычайно обильно: по уровню кровоснабжения (мл/мин/100г массы) миокард уступает только почке и превышает другие органы, включая головной мозг. В частности, этот показатель для сердечной мышцы в 20 раз выше, чем для скелетной.
Лимфатические сосуды в эпикарде сопровождают кровеносные. В миокарде и эндокарде они проходят самостоятельно и образуют густые сети. Лимфатические капилляры обнаружены также в атриовентрикулярных и аортальных клапанах. Из капилляров лимфа, оттекающая от сердца, направляется в парааортальные и парабронхиальные лимфатические узлы.
4 Иннервация сердца
В стенке сердца обнаруживается несколько нервных сплетений и ганглиев. Наибольшая плотность расположения нервных сплетений наблюдается в стенке правого предсердия и синусно-предсердного узла проводящей системы.
Рецепторные окончания в стенке сердца образованы нейронами ганглиев блуждающих нервов и нейронами спинномозговых узлов, а также ветвлениями дендритов равноотростчатых нейроцитов внутриорганных ганглиев (афферентные нейроны).
Пресинаптический аппарат в кардиомиоцитах синапсов характеризуется тем, что практически не удается выделить в миокардиоцитах локальные постсинаптические структуры, так как эффекторные влияния имеют модулирующий характер.
Электротоническое влияния в миокардиальной ткани распространяются далеко за пределы одной клетки, и как следствие, обнаружение высокого коэффициента передачи между кардиомиоцитами, что обусловлено наличием электрических синапсов (щелевых контактов) между клетками. При этом автоматизм сокращения связан с передачей импульса через указанные контакты.
В миокарде много афферентных и эфферентных нервных волокон. Раздражение нервных волокон, окружающих проводящую систему, а также нервов, подходящих к сердцу, вызывает изменение ритма сердечных сокращений. Это указывает на определяющую роль нервной системы в ритме сердечной деятельности, следовательно, и в передаче импульсов по проводящей системе сердца.
5. Функциональная адаптация сердца
Функциональная адаптация клеток в гистогенезе сердечной мышечной ткани проявляется в гетерохромном развитии мышечных элементов миокарда различных отделов сердца. По морфологическим, гистохимическим, гистоавторадиографическим и биометрическим признакам, а также скорости дифференцировки мышечных клеток миокард желудочков, предсердий и мышечные трабекулы отличаются друг от друга, что находится в связи с особенностями гемодинамики, трофики и функции этих отделов миокарда.
Генетически детерминированные основные параметры процессов дифференциации, пролиферации и интеграции клеток миокарда характеризуются известным диапазоном изменчивости, вследствие чего осуществляется адаптация миокарда к конкретным условиям функционировании на каждом этапе фило- и онтогенеза как в норме, так и под влиянием различных внутренних и внешних условий.
6. Возрастные изменения сердечной деятельности
В течение онтогенеза можно выделить три периода изменения гистоструктуры сердца:
В период 20-30 лет при обычной функциональной нагрузке сердце человека находится в стадии относительной стабилизации. В возрасте старше 30-40 лет в миокарде обычно начинается некоторое увеличение его соединительнотканной стромы. При этом в стенке сердца, особенно в эпикарде, появляются адипоциты.
Степень иннервации сердца также изменяется с возрастом. Максимальная плотность внутрисердечных сплетений на единицу площади и высокая активность медиаторов отмечаются в период полового становления человека. После 30-летнего возраста уменьшаются плотность холинергических сплетений и количество медиаторов в них сохраняется на постоянном уровне. Нарушение равновесия в вегетативной иннервации сердца предрасполагает к развитию сложных патологических состояний. В пожилом возрасте уменьшается активность медиаторов в холинергических сплетениях сердца.
При повышенных систематических функциональных нагрузках общее количество клеток не возрастает, но в цитоплазме увеличиваются содержание органелл общего значения и миофибрилл, а также размер клеток (функциональная гипертрофия); соответственно возрастает и степень плоидности ядер кардиомиоцитов.
7. Регенерация сердечной мышечной ткани
Для сердца как органа характерна способность к регенерации путем регенераторной гипертрофии, при которой масса органа восстанавливается, но форма остается нарушенной. Подобное явление наблюдается после перенесенного инфаркта миокарда, когда масса сердца может восстановиться как целое, при этом на месте повреждения образуется соединительнотканный рубец, но орган гипертрофируется, т.е. нарушается форма. Происходит не только увеличение размеров кардиомиоцитов, но и пролиферация в основном в предсердиях и ушках сердца.
Ранее полагали, что дифференцировка кардиомиоцитов является необратимым процессом, связанным с полной потерей этими клетками способности к делению. Но на современном уровне многочисленные данные показывают то, что дифференцированные кардиомиоциты способны к синтезу ДНК и митозу. В исследовательских работах П.П. Румянцева и его учеников показано, что после экспериментального инфаркта миокарда левого желудочка сердца в клеточный цикл возвращается 60-70% предсердных кардиомиоцитов, возрастает число полиплоидных клеток, но это не компенсирует повреждение миокарда.
Установлено, что кардиомиоциты способны к митотическому делению (в том числе и клетки проводящей системы). В миокарде сердца особенно много одноядерных полиплоидных клеток с 16-32-кратным содержанием ДНК, но встречаются и двуядерные кардиомиоциты (13-14%) в основном октоплоидные.
В процессе регенерации сердечной мышечной ткани кардиомиоциты участвуют в процессе гиперплазии и гипертрофии, возрастает их плоидность, но уровень пролиферации клеток соединительной ткани в области повреждения оказывается в 20-40 раз выше. В фибробластах активизируется синтез коллагена, в результате чего репарация происходит путем рубцевания дефекта. Биологическое представление подобной адаптационной реакции соединительной ткани объясняется жизненной важностью сердечного органа, так как задержка с закрытием дефекта может привести к гибели.
Считалось, что у новорожденных, а возможно, и в раннем детском возрасте, когда способные к делению кардиомиоциты еще сохраняются, регенераторные процессы сопровождаются увеличением количества кардиомиоцитов. При этом у взрослых физиологическая регенерация осуществляется в миокарде в основном путем внутриклеточной регенерации, без увеличения количества клеток, т.е. в миокарде взрослого человека отсутствует пролиферация кардиомиоцитов. Но недавно получены данные о том, что в здоровом сердце человека 14 миоцитов из миллиона находится в состоянии митоза, завершающегося цитотомией, т.е. количество клеток не значительно, но увеличивается.
Применение современных методов клеточной биологии в клинических и экспериментальных исследованиях позволило перейти к выяснению клеточных и молекулярных механизмов повреждения и регенерации миокарда. Особенно интересны данные о том, что в перинекротических областях и в функционально перегруженном сердце происходит синтез эмбриональных миоакрдиальных белков и пептидов, а также белков, синтезирующихся во время клеточного цикла. Это подтверждает положение о сходстве механизмов регенерации и нормального онтогенеза.
Выяснилось также и то, что дифференцированные кардиомиоциты в культуре способны к активному митотическому делению, что, возможно, объясняется не полной утратой, а подавлением способности кардиомиоцитов возвращаться в клеточный цикл.
Важной задачей теоретической и практической кардиологии является разработка способов стимуляции восстановления поврежденного миокарда, т.е. индукции миокардиальной регенерации и уменьшения соединительнотканного рубца. Одно из направлений исследований предоставляет возможность переноса регуляторных генов, которые превращают фибробласты рубца в миобласты или трансфекция в кардиомиоциты генов, контролирующих рост новых клеток. Другим направлением является перенос в область повреждения фетальных скелетных и миокардиальных клеток, которые могли бы участвовать в восстановлении сердечной мышцы. Также проводятся эксперименты по трансплантации скелетной мышцы в сердце, показывающие образование в миокарде участков сокращающейся ткани и улучшающие функциональные показатели миокарда. Перспективным может быть лечение с применением факторов роста, оказывающих как прямое, так и косвенное воздействие на поврежденный миокард, например, улучшение ангиогенеза.
8. Патологическая гистология сердечной мышечной ткани
Различные повреждающие воздействия на сердце (прекращение притока артериальной крови, травмы, воспаления и др.) могут вызвать некроз мышечной ткани, т.е. гибель мышечных клеток. Некроз, возникающий при нарушении или прекращении кровотока в артериях вследствие тромбоза, эмболии, длительного спазма или в условиях недостаточного коллатерального кровообращения, более характерен для миокарда. Артериальная сеть поперечнополосатых мышц в большом количестве имеет анастомозирующие сосуды, поэтому в случае полного закрытия артерии ишемии не наблюдается. Дистрофические и некротические изменения в мышцах развиваются только при длительном закрытии крупных артерий.
Для миокарда характерны следующие клинико-морфологические формы некроза: коагуляционный некроз, коагуляционный миоцитолиз, колликвационный некроз. В развитии разных типов некроза участвуют различные биохимические механизмы.
Колликвационный некроз развивается в результате пропитывания миокарда экссудатом из кровеносных сосудов. При этом в клетках возникает внутриклеточный отек и вакуолизация, что обычно может наблюдаться в периваскулярной и субэндотелиальной областях после инфаркта.
Вследствие воспалительной реакции происходит рассасывание омертвевшей мышечной ткани и последующим замещением рубцом. Вокруг пораженного участка наблюдается жировая дистрофия и липоматоз, а также отложение извести.
При атрофии миокарда тяжи кардиомиоцитов постепенно становятся тоньше. В случае сильной атрофии исчезает поперечная исчерченость, продольная же сохраняется дольше. В местах атрофии может развиться воспалительный процесс, образование межуточной соединительной ткани.
Наиболее типичной приспособительной реакцией миокарда на повышение физической нагрузки является гипертрофия. Гипертрофия сердечной мышцы часто относится к рабочим гипертрофиям, при этом наблюдается утолщение мышечных волокон и кардиомиоцитов, обусловленное увеличением количества саркоплазмы и миофибрилл. Установлено, что в миокарде гипертрофия является реакцией на пролиферативные стимулы и гемодинамическую нагрузку кардиомиоцитов, вышедшие из митотического цикла (исследования гипертрофии миокарда при различных воздействиях: бег, плавание, индивидуальные дозированные физические нагрузки, экспериментальная коарктация аорты и др.)
Процесс гипертрофии включает три основных стадии:
2. Стадия завершающейся гипертрофии и относительной устойчивости гиперфункции;
3. Стадия прогрессирующего кардиосклероза и постепенного истощения при явлениях нарушения синтеза нуклеиновых кислот и белков.
Заключение
Анализ структурно-функциональных особенностей сердечной мышечной ткани показал, что, несмотря на то, что миокардиальная ткань состоит из отдельных клеток, в функциональном отношении она представляет собой единую систему. Способность сердечной мышечной ткани к регенерации, а также адаптация миокарда к конкретным условиям функционирования позволяют по-новому посмотреть на вопросы лечения и профилактики заболеваний сердечно-сосудистой системы, возникновение которых связано с повреждением структуры сердечной мышечной ткани и, как следствие, дисфункцией сердечной деятельности.
На современном уровне полагают, что в проблеме микроциркуляции заложен целый ряд расстройств сердечно-сосудистой деятельности при различных заболеваниях организма. Данная область получила ускоренное развитие особенно во 2-й половине ХХ века и уже сегодня формирует новые принципы в лечении патологий сердца. Импульсом к этому послужило техническое совершенствование исследований трансорганной микрогемодинамики и разработка методологических подходов к анализу гемато-тканевых взаимодействий в системе микроциркуляции.
Проведение научных исследований в различных направлениях, в том числе и микроциркуляционного русла сердца, совершенствование существующих и развитие новых способов оперативного лечения врожденных и приобретенных пороков сердца, применение современного диагностирующего оборудования и эффективных лекарственных препаратов, а также просвещение общества в направлении здорового образа жизни представляют возможность достижения целей, направленных на обеспечение лечения заболеваний сердечно-сосудистой системы и сохранение здоровья человека.
3. Куприянов В.В., Караганов Я.Л., Козлов В.И. Микроциркуляторное русло. М.: Медицина, 1975.