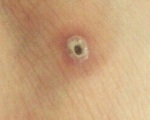
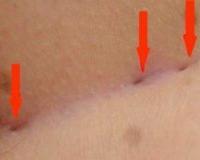
Свищ ( Фистула )
Свищ – это патологический канал, который соединяет между собой полые органы, естественные или патологические полости тела между собой (внутренний свищ) либо с окружающей средой (наружный свищ). Проявляется наличием свищевого хода, через который выделяется слизь, гной, содержимое органа или полости: кал, моча, слюна, ликвор, желчь. Диагностируется на основании клинической симптоматики, данных фистулографии, других инструментальных и лабораторных исследований. При внутренних свищах проводятся эндоскопические манипуляции. Лечение определяется видом патологии, может быть консервативным, оперативным, комбинированным.
МКБ-10
Общие сведения
Свищи (фистулы) – большая и весьма разнородная группа патологических состояний, встречающихся во многих сферах практической медицины. Они имеют врожденный или приобретенный характер, возникают в результате разрушения тканей различного генеза либо создаются искусственно. Нередко тяжело поддаются лечению, в ряде случаев представляют опасность для жизни из-за значительных потерь жидкости, питательных веществ. Наибольшее клиническое значение вследствие своей распространенности и возможных последствий имеют урогенитальные и желудочно-кишечные свищи.
Причины свищей
Непосредственной причиной образования фистул являются нарушения формирования либо разрушение органов и тканей. С учетом этиологии выделяют следующие группы свищей:
Патогенез
Врожденные свищи становятся следствием недоразвития или неправильного развития органов и частей тела. Поскольку они образуются естественным путем, их стенки покрыты эпителием. Приобретенные фистулы появляются при прорыве содержимого, сопровождаются разрушением уже сформированных тканей. Стенки представлены грануляциями, снаружи в результате рубцевания со временем образуется прослойка из плотной соединительной ткани.
Особой группой являются губовидные свищи, у которых эпителий слизистой переходит в эпителий кожных покровов. Они относятся к эпителизированным, но создаются искусственно. Эпителизированные свищи самостоятельно не закрываются. Гранулирующие фистулы способны к заживлению при устранении процесса (обычно – воспалительного), поддерживающего отток содержимого по каналу.
Классификация
В настоящее время исследователи, а также специалисты в области хирургии используют следующую систематизацию свищей:
Симптомы свища
Общим признаком заболевания является наличие патологического сообщения между двумя или более полостями либо полостью организма и окружающей средой. При наружных свищах в ходе осмотра выявляется отверстие (ход). Края отверстия воспалены, мацерированы из-за раздражения кожи. Количество и характер отделяемого различаются в зависимости от вида свища, особенностей патологического процесса.
Внутренние фистулы проявляются наличием нетипичного отделяемого из какого-либо естественного отверстия. Значительные потери жидкости и питательных веществ при некоторых типах свищей становятся причиной истощения, грубых нарушений всех видов обмена, которые могут привести к гибели пациента.
Свищи пищеварительной системы
Могут образовываться на всем протяжении ЖКТ, от пищевода до прямой кишки, быть наружными либо внутренними. Желудочные фистулы обычно имеют искусственное происхождение (гастростома), пищеводные провоцируются патологическим процессом, кишечные бывают искусственными (колостома, илеостома, цекостома) и патологическими. Первое место среди причин образования пищеводных свищей занимают опухоли, кишечных – несостоятельность анастомозов.
Формирование наружных свищей сопровождается появлением инфильтрата. При внутренних фистулах клиническая картина напоминает прободение полого органа. При трахеопищеводных соустьях из верхних дыхательных путей откашливаются кусочки пищи. Внутренний желудочно-кишечный свищ проявляется каловой рвотой, каловым запахом изо рта. При наружном сформированном свище на коже обнаруживается ход с пищеводным, желудочным или кишечным отделяемым, при несформированном – гнойная рана, на дне которой видна петля кишки, стенка желудка.
Типичны поносы, рвота, аутоинтоксикация. Скорость истощения и развития обменных нарушений зависит от диаметра свища – чем он шире, тем быстрее усугубляется симптоматика. Возможны обезвоживание, истощение, безбелковые отеки, анемия. Интоксикация, расстройства обмена приводят к изменениям со стороны печени и почек. В тяжелом случае развиваются почечная и печеночная недостаточность.
Свищи желчного пузыря
Желчные свищи обычно становятся осложнением желчнокаменной болезни, бывают наружными или внутренними, могут соединять желчевыводящие пути с желудком, кишкой, плевральной полостью, бронхом. Наружные свищи сопровождаются образованием отверстия с желчным либо гнойным отделяемым, внутренние – симптомами холангита, поносами, потерей веса, интоксикацией.
Ректальные свищи
Включают различные формы парапроктита и ректовагинальные фистулы. Парапроктит возникает при гнойном воспалении стенки кишки и параректальной клетчатки, проявляется болями, ощущением инородного тела, общими симптомами интоксикации. Из заднего прохода выделяется гной либо на коже перианальной зоны обнаруживается отверстие с гнойным отделяемым. При ректовагинальных свищах из влагалища выделяются газы, кал. Нередки боли в промежности, воспалительные заболевания половых органов, мочевыводящих путей.
Урогенитальные свищи
Образуются между половыми органами и уретрой, мочеточниками или мочевым пузырем. Развиваются после тяжелых и осложненных родов, операций, лучевой терапии. Наиболее распространенные – уретро-влагалищные и пузырно-влагалищные фистулы. Реже встречаются пузырно-маточные, мочеточниково-влагалищные и другие варианты.
Сопровождаются подтеканием мочи из половых органов, появлением крови в моче во время менструаций. Обычно безболезненны. Не представляют угрозы для жизни, но существенно снижают ее качество, становятся причиной социальной дезадаптации. Имеют большое клиническое значение из-за высокой распространенности (0,6-2%).
Бронхиальные свищи
Чаще возникают после операций на легких, характеризуются появлением сообщения с кожей, плевральной полостью или полыми органами – пищеводом, желудком, кишечником, желчным пузырем. Проявляются одышкой, кашлем, выделением гноя или нетипичного содержимого (пищи, желчи) из дыхательных путей, слабостью, потливостью, повышением температуры тела.
Лигатурные свищи
Осложнения
Наиболее распространенными осложнениями любых свищей являются гнойные и негнойные воспалительные процессы, в том числе – образование абсцессов и затеков с поражением соседних анатомических структур, хронические воспаления различных органов (циститы, вагиниты, проктиты). В тяжелых случаях возможен сепсис.
Свищи значительно ухудшают качество жизни, часто становятся причиной потери трудоспособности, негативно влияют на социализацию. При наружных фистулах нередко развиваются дерматиты, формируется косметический дефект. При полных свищах внутренних органов наблюдается кахексия, полиорганная недостаточность.
Диагностика
С учетом локализации свища диагноз устанавливают врачи различных специальностей – хирурги, гинекологи, урологи и пр. В процессе диагностики и определения плана лечения учитывают историю болезни, клиническую симптоматику, данные дополнительных исследований. План обследования включает:
Некоторые внутренние свищи представляют существенные диагностические затруднения, обнаруживаются только при проведении оперативных вмешательств. Дифференциальную диагностику проводят между различными видами фистул, с воспалительными заболеваниями, другими патологическими процессами.
Лечение свища
Тактика лечения определяется видом фистулы. Гранулирующие свищи могут закрываться на фоне консервативной терапии, при эпителизированных выздоровление возможно только после осуществления оперативного вмешательства. Наряду с устранением основной патологии важную роль играет коррекция обменных нарушений, грамотный уход за отверстием.
Консервативная терапия
Обязательным условием закрытия свища является устранение причины его появления. При невозможности воздействия на этиологический фактор целью терапии становится подготовка больного к операции. Лечение предусматривает проведение общих и местных мероприятий. Показано в случае всех видов свищей – как эпителизированных, так и гранулирующих. Включает:
Хирургическое лечение
Хирургические вмешательства проводятся при эпителизированных, сформированных гранулирующих, губчатых свищах. С учетом особенностей расположения фистулы и состояния окружающих тканей выполняются следующие операции:
Удаление измененных тканей нередко дополняют действиями, направленными на предотвращение повторного образования свища. Для этого между разобщенными полостями помещают участки фасции, сетчатые имплантаты. В послеоперационном периоде проводят стандартные лечебные мероприятия – перевязки, антибиотикотерапию, обезболивающую терапию.
Прогноз
Прогноз определяется локализацией, видом и временем существования свища, распространенностью изменений окружающих тканей, характером основной патологии, степенью нарушения гомеостаза организма больного, наличием сопутствующих заболеваний. Фистулы, даже гранулирующие, редко поддаются консервативному лечению. После иссечения достаточно часто наблюдается выздоровление. При некоторых видах свищей, сопровождающихся тяжелыми обменными нарушениями, особенно – при высоких желудочно-кишечных, возможен летальный исход.
Профилактика
Профилактические мероприятия включают своевременное лечение заболеваний, которые могут приводить к образованию свищей. Необходимо предупреждать возникновение инфекций в зоне раневых каналов, соблюдать технику наложения анастомозов, обеспечивать разгрузку оперируемых органов на этапе подготовки к вмешательству и послеоперационного восстановления.
Лечение лигатурного свища в Москве стоимость
Лечение лигатурного свища в Москве стоимость
Лигатурный свищ возникает вследствие воспаления и нагноения нерассасывающихся хирургических нитей, которыми с
шиты ткани (фасции и др.) при различных операциях.
При оперативных вмешательствах часть тканей (мышцы, подкожная клетчатка) сшивают рассасывающимися нитями, а часть (апоневроз, сухожилия и др.) – нерассасывающимися, т.к. такие ткани срастаются медленно и подвержены большим нагрузкам. Как правило, нерассасывающиеся нити навсегда остаются в тканях, не вызывая каких-либо проблем, но в редких случаях нагнаиваются, тогда в области нити появляется небольшой абсцесс, который вскрывается через маленькое отверстие на коже и формируется свищ.
Причины лигатурных свищей
Основная причина появления лигатурных свищей – инфицирование нити. Чаще всего оно происходит при операциях на полых органах – кишка, желудок, желчный пузырь и др. При этих вмешательствах просвет полых органов вскрывают и даже при самом корректном проведении операции инфицирования в той или иной степени избежать не удается. Иногда бывает, что инфицирование вызывается несоблюдением правил асептики при операции либо некачественным шовным материалом, но такие случаи довольно редки. Далее все зависит от агрессивности микроба, иммунного статуса организма. Если микробный агент агрессивен, а иммунных сил недостаточно для его подавления, происходит нагноение нити. Если нить нагноилась, то до отторжения нити гнойный процесс не прекращается, то обостряясь, то затихая.
Симптомы, диагностика лигатурного свища
Лигатурный свищ появляется в разные сроки после операции – от нескольких дней до нескольких месяцев и даже лет. В области послеоперационного рубца возникает покраснение, умеренные боли, может повышаться температура тела. Эти явления связаны с нагноением и появлением скопления гноя под кожей – лигатурного абсцесса. Через несколько дней абсцесс самопроизвольно прорывается на коже в области рубца, вытекает гной, и на коже остается небольшое отверстие с подтеканием мутноватой жидкости – это и есть лигатурный свищ. Если нагноилась не одна нитка, свищей может быть несколько. На фоне лечения свищ может закрываться, но если нитка не отторглась (не вышла наружу), свищ неизбежно открывается вновь. Так, периодически то открываясь, то закрываясь, свищ может существовать несколько месяцев и даже лет, пока нить не отторгнется сама, либо будет удалена хирургом.
Лечение лигатурного свища
При начальных проявлениях в виде лигатурного абсцесса производят небольшой надрез кожи для оттока гноя, т.к. ждать пока гной прорвется сам нецелесообразно в связи с риском нагноения окружающих тканей и формирования флегмоны – разлитого воспаления подкожной клетчатки. После вскрытия гнойника обычно пытаются вслепую достать зажимом лигатуру. Если это удается, то после очищения раны свищ закрывается навсегда. Если лигатуру достать не получается, назначают перевязки с мазью левомеколь, на фоне которых воспаление стихает, свищ может временно закрыться. При новом воспалении опять пытаются достать лигатуру, рано или поздно это удается. Можно сделать широкий разрез в области свища, попытаться найти воспаленную нить и удалить ее, но это не всегда получается, к тому же во время обширного вмешательства существует риск инфицирования соседних нитей с последующим формированием новых свищей.
Подводя итог вышесказанному, можно сказать, что лигатурный свищ – редкое осложнение полостных и других хирургических вмешательств, которое не опасно для жизни, но может беспокоить пациента довольно долго, вплоть до отторжения или удаления нагноившейся нити.
Лечение свищей
Свищ (фистула) – это патологический канал. Он соединяет между собой две полости тела или какой-то орган с внешней средой. Свищ появляется, когда в очаге инфекции накапливается гнойная жидкость. Жидкость не помещается в своей полости, поэтому образуется своеобразная трубка для ее выхода наружу. Фистула может быть внутренней (в органах) и наружной (на коже).
Лечением свищей и проведением операций по их поводу занимается хирург. Запишитесь на консультацию по телефону 8 (831) 212-77-77 или онлайн. Стоимость приема от 1.100 рублей.
Как проявляет себя свищ:
Свищ – это не только эстетический дефект, лечить его нужно обязательно. Он вызывает различные опасные воспаления. Это могут быть абсцессы или хронические заболевания – вагинит, проктит, цистит. Возможен даже сепсис. Свищ снижает качество жизни, мешает нормальной активности, работе. Если фистула затронула нервные окончания, пораженное место будет сильно болеть.
Лечения свищей в Клинике семейного врача
Лечением свищей занимается хирург. Что предлагает Клиника семейного врача для хирургического избавления от свищей:
Цены на услуги хирургии в «Клинике семейного врача»
Цены, указанные на сайте, не являются публичной офертой. Стоимость услуг устанавливается и оплачивается согласно прейскуранту Клиники, действующему на момент оказания соответствующей услуги. С действующим прейскурантом Вы можете ознакомиться на стойке регистратуры, у администратора или по телефону
212-77-77.
Уважаемые посетители нашего сайта! Данная статья посвящена хирургическому лечению гнойно–воспалительных заболеваний суставов, осложненных деструкцией костной ткани (остеомиелитом), гнойным осложнениям эндопротезирования.
Данная группа заболеваний является серьезной, не решенной окончательно проблемой современной ортопедии. Единые стандарты лечения данной патологии отсутствуют. Подходы к лечению базируются на личном опыте отдельных авторов и клиник. Мы бы хотели осветить принципиальные моменты диагностики данной группы заболеваний и поделиться личным опытом их лечения.
Частота встречаемости септических артритов составляет от 2 до 10 случаев на 100 000 населения. Преобладает поражение коленного сустава (до 55%), затем следуют тазобедренный и голеностопный суставы. Страдают подобными заболеваниями преимущественно дети и пожилые люди.
Каковы предпосылки развития гнойных артритов? Это травмы области суставов, дегенеративные и ревматоидные заболевания суставов, выполнение инъекций в области сустава, артроскопических вмешательств, эндопротезирование сустава в анамнезе, гнойно-воспалительные заболевания, трофические язвы дистальных отделов конечностей, инфекции, передающиеся половым путем, системный прием препаратов глюкокортикоидов.
Клиническая картина заболевания. Проявления заболевания достаточно отчетливы при поражении суставов, близко расположенных к коже (локтевой, коленный, голеностопный). Это отек тканей в области сустава, местное покраснение и повышение температуры кожи. При поражении крупных, глубоко лежащих суставов, таких как плечевой и тазобедренный, местные изменения могут быть не выражены, и пациента будет беспокоить только боль в области сустава. Повышение температуры тела также может появиться не сразу. На представленной ниже фотографии типичная клиническая картина артрита коленного сустава: контуры правого коленного сустава сглажены, сустав увеличен в объеме.
Лабораторная диагностика заболевания. В объем обследования пациента с подозрением на гнойный процесс обязательно должны входить клинический анализ крови с подсчетом лейкоцитарной формулы и скорости оседания эритроцитов, анализ крови на С-реактивный белок. Среди лабораторных показателей хочется отдельно остановиться на уровне прокальцитонина. Прокальцитониновый тест в настоящее время является наиболее объективным методом определения генерализации бактериального инфекционного процесса. Динамическое повышение данного показателя в анализах крови пациента является показателем распространения гнойного процесса за пределы сустава, развития сепсиса.
Лечение. При лечении гнойно – воспалительных заболеваний суставов нашей задачей является скорейшее купирование воспалительного процесса и, по возможности, сохранение функции сустава. По данным различных авторов, при гнойном процессе в суставе, суставной хрящ поражается на 4 – 6 сутки от начала заболевания и окончательно отмирает на 4-й неделе заболевания, после чего эффективность сохраняющих сустав операций резко снижается. При отсутствии признаков поражения костной ткани в настоящее время предпочтение отдается операциям, сохраняющим сустав. При поражении поверхностно расположенных суставов на ранних стадиях заболевания возможно использование пункционных методов и антибиотикотерапии широкого спектра действия. При неэффективности пункционных методов в течение 48 часов от начала заболевания рекомендовано выполнение дренирования сустава. В идеале – к этому склоняется большинство современных авторов – использование артроскопических методик.
Наш личный опыт: лечение септического артрита голеностопного сустава у 19-летнего пациента путем 3-х недельного проточно – промывного дренирования. Промывная система была установлена через доступы до 2-х см. Результат лечения – полное купирование воспалительного процесса, выздоровление пациента. За два года последующего наблюдения рецидива заболевания не отмечено. При распространении гнойного процесса на костную ткань выполняется удаление нежизнеспособных тканей и стабилизация области сустава с помощью аппарата наружной фиксации. В результате воспалительный процесс купируется и формируется артродез пораженного сустава, т. е сращение между костями, формирующими сустав, что обеспечивает в последующем адекватную опорную функции конечности.
Личный опыт: Пациентка, 81 год, поступила в клинику с болями в области тазобедренного сустава, беспокоившими в течение 4х месяцев, после падения с высоты роста. В течение недели перед поступлением в клинику боли неуклонно нарастали, нарушилась опорная функция конечности. Повышения температуры тела не отмечала, постоянно принимала противовоспалительные препараты (мовалис) в больших дозах.
Рентгенограмма при поступлении.
Определяются зоны деструкции в теле подвздошной кости, в головке бедренной кости.
При пункции тазобедренного сустава – густое гнойное содержимое.
В экстренном порядке пациентка прооперирована: вскрыт сустав, санирован очаг остеомиелита, удалена головка бедренной кости, сустав фиксирован стержневым внеочаговым аппаратом. Установлена система проточно–промывного дренирования. В течение 6ти недель пациентке проводилась терапия антибиотиками широкого спектра действия. На фоне лечения купированы боли в области тазобедренного сустава, в клинико–лабораторных тестах – снижение показателей воспалительного ответа.
Аппарат внешней фиксации демонтирован через 8 недель после операции. Тазобедренный сустав фиксирован ортопедическим фиксатором. Через 3 месяца после операции фиксатор снят. Пациентка самостоятельно ходит с полной нагрузкой на оперированную ногу. Воспалительный процесс купирован.
Результаты спиральной компьютерной томографии костей таза пациентки через 3 месяца после операции.
Определяются признаки формирования сращения между бедренной костью и телом подвздошной кости. Данное сращение обеспечивает в будущем адекватную опорную функцию конечности.
При ранних глубоких нагноениях после эндопротезирования тазобедренного сустава возможно сохранение эндопротеза. Хроническая инфекция области эндопротеза и деструктивный остеомиелит у взрослых, развившийся на фоне септического артрита являются показаниями для радикальной хирургической санации, удаления компонентов эндопротеза, некротизированных участков костной ткани.
Клинический пример: Пациентка 65 лет. В анамнезе тотальное эндопротезирование тазобедренного сустава, выполненное заграницей в 2002 году. Динамического наблюдения за суставом не осуществлялось. В течение последних двух лет с 2012 года беспокоят периодические боли в области тазобедренного сустава. С сентября 2013 года, в течение 3х месяцев отмечает постепенное усиление болей. За две недели до поступления в клинику на дому осуществлялся массаж области сустава, иглорефлексотерапия. После курса указанных процедур отмечено резкое усиления болей, подъем температуры тела до 39 градусов.
Рентгенограммы пациентки при поступлении.
Определяются признаки деструкции вертлюжного компонента протеза, признаки деструкции костной ткани по ходу бедренного компонента протеза.
При пункции сустава получено густое гнойное содержимое Выполнено вскрытие полости сустава, удаление компонентов эндопротеза, радикальная обработка очага остеомиелита. При ревизии выявлено гнойное расплавление проксимального отдела бедренной кости. Установлен артикулирующий спейсер.
Рентгенограмма пациентки после операции.
Модель проксимального отдела бедра сформирована из костного цемента с антибиотиками, армирована проксимальным бедренным стержнем.
Послеоперационное течение гладкое. Воспалительный процесс купирован. Планируется выполнение реэндопротезирования. Данный клинический пример ярко демонстрирует необходимость своевременного обращения к специалисту травматологу – ортопеду и недопустимость выполнения физиотерапевтических процедур без предварительной адекватной диагностики причины болей в области суставов.
Специалисты Ортоцентра владеют всеми методами оперативного лечения гнойно – воспалительных заболеваний суставов и готовы прийти к Вам на помощь.
ФЛЕГМОНЫ И АБСЦЕССЫ — современные возможности лечения
В чем трудность лечения флегмон и абсцессов? Почему нецелесообразно применять мази на вазелиново-ланолиновой основе? Какие местные препараты соответствуют современным представлениям о лечении флегмон и абсцессов? Несмотря на активное внедрение
В чем трудность лечения флегмон и абсцессов?
Почему нецелесообразно применять мази на вазелиново-ланолиновой основе?
Какие местные препараты соответствуют современным представлениям о лечении флегмон и абсцессов?
Несмотря на активное внедрение в клиническую практику новых групп антибиотиков, проблема профилактики и лечения гнойно-септических осложнений в хирургии по-прежнему актуальна. Так, согласно литературным данным, частота гнойно-воспалительных осложнений после грыжесечений достигает 28,3%, после резекций желудка — 28,4%, холецистэктомий — 32%, аппендэктомий — 40,4%, панкреатитов — 50% (Прискарь В. И., 1999).
Летальность при перитоните колеблется от 16 до 80% (Даценко Б. М. с соавт., 1998, Гельфанд Б. М. с соавт., 1999, Камзакова Н. И., 2000).
В структуре внутрибольничных инфекций послеоперационные инфекции составляют 12,2%, а постинъекционные инфекции — 17%. Необходимо отметить, что процент тяжелых последствий внутрибольничных инфекций практически одинаков для хирургических стационаров и амбулаторно-поликлинических учреждений — 15,2% и 15,6% соответственно.
Особую тревогу вызывают случаи запоздалой диагностики осложненного течения абсцессов или флегмон. Так, например, в зависимости от локализации первичного гнойного процесса могут формироваться тяжелые гнойные артриты (после внутрисуставного введения гормональных, обезболивающих препаратов), тромбофлебиты (после внутрисосудистого введения различных лекарственных средств) с последующей генерализацией инфекционного процесса, с формированием гнойных очагов во внутренних органах (в сердце, легких, почках).
Ретроспективный анализ тяжелых абсцессов и флегмон, осложнившихся сепсисом после длительного консервативного или недостаточно активного хирургического вмешательства, показывает, что одной из основных причин возникновения осложнений можно считать недостаточное внимание к ранней диагностике формирующихся абсцессов и флегмон различной локализации, предполагающей использование современных неинвазивных методов исследования (ультразвука, компьютерной томографии), а также инвазивных диагностических методов, и прежде всего диагностической пункции области инфильтрата. Особую тревогу вызывает так называемая выжидательная тактика, когда, выполнив диагностическую пункцию и удалив некоторое количество гноя, хирурги пытаются дренировать гнойную полость с помощью резиновой трубки и назначают какой-либо антибактериальный препарат.
Радикальные оперативные вмешательства на уже сформированном гнойном очаге выполняются слишком поздно, дренирование послеоперационной раны бывает, как правило, неадекватным.
Кроме того, не уделяется должного внимания проблеме асептики и антисептики при оказании помощи пострадавшим, а также при выполнении различных диагностических и лечебных манипуляций как на амбулаторно-поликлиническом, так и стационарном этапах лечения. Использование традиционных антисептиков в данных ситуациях, к сожалению, не предупреждает развитие инфекционного процесса, так как проблема устойчивости микроорганизмов в равной степени актуальна как для группы антибактериальных препаратов, так и для традиционных антисептиков.
К примеру, чувствительность S.aureus, E.coli, B.fragilis к раствору фурациллина составляет менее 3, 1 и 3% соответственно. Массивность контаминации P.aeruginosa в растворе фурациллина может достигать 106 КОЕ/мл. Частота контаминации раствора фурациллина грибами достигает 58%.
В табл. 1 приводится далеко не полный перечень традиционных препаратов, от которых необходимо отказаться полностью и которые, тем не менее, используются как в домашних условиях, так и в медицинских учреждениях.
В данном сообщении приводится анализ результатов лечения 166 больных с постинъекционными флегмонами и абсцессами в специализированном отделении ран и раневой инфекции Института хирургии им. А. В. Вишневского РАМН. Больных, как правило, переводили из других хирургических стационаров ввиду прогрессирующего нарастания клиники интоксикации, с полиорганной недостаточностью, с сепсисом.
Возраст пациентов колебался от 18 до 84 лет. 124 больных были в возрасте от 30 до 60 лет. Длительность лечения на предыдущем этапе от начала формирования гнойного процесса составляла от 12 суток до 1,5 месяцев.
Сопутствующие заболевания: гипертоническая болезнь — 46 больных, остеохондроз тазобедренных суставов — 31 пациент, пояснично-крестцовый радикулит — 27 больных, почечная колика — 16 и другие заболевания — 46.
Гнойно-воспалительные процессы возникали после введения обезболивающих препаратов (анальгина, баралгина), гипотензивных (папаверина с дибазолом, магнезии), гормональных препаратов, кордиамина, масляных растворов витаминов, кокарбоксилазы и др.
Инфекционный процесс в 139 случаях возникал после инъекций, выполненных медицинскими работниками (бригады «скорой помощи», процедурные и хирургические кабинеты поликлиник, стационары). В остальных 27 случаях препараты вводились в домашних условиях не медицинскими работниками. Локализация абсцессов: в подавляющем большинстве случаев — это места внутримышечных инъекций (ягодичные области, реже — предплечья и места паранефральных, паравертебральных блокад).
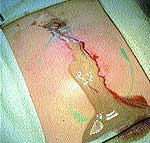 |
| Рис. 1 |
При первичном обращении больного за помощью по месту жительства в случае появления первых признаков формирования воспалительного процесса в качестве препаратов первой помощи использовались 3%-ный раствор йода («йодная сетка»), компрессы со спиртом, мазью Вишневского, ихтиоловой мазью. Консервативное медикаментозное лечение с подключением физиотерапевтических методов иногда продолжалось до 2–3 недель (рис. 1).
В дальнейшем, уже в условиях хирургических стационаров после хирургического вмешательства, послеоперационные раны тампонировались либо марлевыми тампонами, пропитанными 10%-ным раствором хлорида натрия, мазью Вишневского, раствором фурациллина, либо с дренирующей целью в раны устанавливались перчаточные резинки или резиновые трубки.
Такой метод лечения быстро приводил к распространению гнойного процесса за пределы первичной локализации, нарастанию интоксикации, развитию сепсиса.
Ввиду неэффективности лечения после развития септического состояния больные переводились для дальнейшего лечения в специализированное отделение гнойной хирургии им. А. В. Вишневского.
При поступлении практически все больные сразу помещались в блок интенсивной терапии отделения гнойной хирургии, где они получали необходимую пред- и послеоперационную корригирующую медикаментозную терапию.
В Институте хирургии им. А. В. Вишневского РАМН разработан метод активного хирургического лечения гнойных ран, основанный на следующих принципах:
Использование вышеперечисленных дополнительных методов воздействия на раневую поверхность позволяет уменьшить обсемененность раневой поверхности патогенной флорой до уровня ниже «критического» — с 10 7-9 до 10 2-3 микробных тел в 1 г ткани раны.
Клинические примеры закрытия ран с помощью швов, дренирования и окончательный результат приведены на рис. 2, 3, 4.
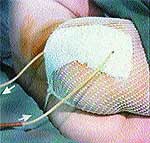 |
| Рис. 3 |
Во время поступления больного в отделение, а также в процессе лечения (во время перевязок, при повторных хирургических обработках ран, перед окончательным закрытием ран) проводятся бактериологические исследования видового состава ран. Результаты представлены в табл. 2.
Как видно из табл. 2, в подавляющем большинстве случаев из ран была выделена грамположительная микрофлора и в единичных случаях — ассоциация грамположительных и грамотрицательных микроорганизмов. Обращает на себя внимание достаточно большое число случаев выявления в ранах неклостридиальной анаэробной инфекции.
 |
| Рис. 4 |
Все штаммы, выделенные из послеоперационных ран больных, ранее прооперированных в других лечебных учреждениях, были полирезистентны к традиционно используемым антибактериальным препаратам, что указывает на госпитальную принадлежность инфекции.
С учетом видового характера выделяемой из ран микрофлоры и чувствительности ее к антибактериальным препаратам назначались общая и местная антибактериальная терапии.
Наиболее часто (38,5%) использовались полусинтетические пенициллины (карбенициллин, ампиокс, диклоксациллин), в 15,7% случаев — аминогликозиды (гентамицин, тобрамицин, сизомицин, нетилмицин), в 12,5% — фторхинолоны (офлоксацин, пефлоксацин, ципрофлоксан), в 10,3% — цефалоспорины (цефотаксим, цефтазидим, цефтриаксон).
При обнаружении гнойно-воспалительного процесса, вызванного неклостридиальной анаэробной инфекцией (27 больных — 16,3%), как правило, назначалась комбинированная антибактериальная терапия — метронидазол с гентамицином или нетилмицином либо клиндамицин с гентамицином или нетилмицином. В последние годы в подобных ситуациях препаратом выбора считается имипенем, позволяющий активно воздействовать как на аэробный, так и анаэробный компонент микрофлоры ран. При локальном гнойном процессе, в случае выявления чувствительности стафилококков к фузидину, назначение этого препарата в комплексном лечении было также оправданно.
Выбор антисептиков, используемых для промывания ран
Как уже было сказано, использование раствора фурациллина в настоящее время нецелесообразно ввиду его крайне низкой антимикробной активности. В настоящее время перспективными можно считать растворы диоксидина, мирамистина, фурагина растворимого.
Прежде всего, очень важно следить за чистотой не только самой раны, но и окружающей рану кожи.
При выборе кожных антисептиков, используемых как с профилактической, так и лечебной целью, предпочтение отдается препаратам с универсальным, широким или умеренным спектром действия, активным против смешанной микрофлоры и обладающим микробоцидным или микробостатическим действием.
1%-ный йодовидон, 1%-ный йодопирон — йодофоры, представляющие собой комплекс поливинилпиролидона с йодом. Различия между этими препаратами связаны со способом их получения, а также разной молекулярной массой поливинилпиролидона. Растворы йодовидона более стабильны при хранении, чем растворы йодопирона, готовящиеся обычно ex tempore. По степени бактерицидного действия эти препараты практически идентичны.
Сульйодопирон представляет собой пенистую жидкость, которая предназначена для мытья грязных инфицированных ран, лечения ран под повязкой, обработки рук хирурга и операционного поля. Сульйодопирон при местном применении оказывает бактерицидное действие.
Бактерицидный эффект при микробной нагрузке 106-107 бактерий на 1 мл среды наступает в течение 1-4 минут, превосходя по этим показателям растворы йодопирона.
1%-ный диоксидин обладает выраженной активностью против большинства аэробных, анаэробных и факультативно анаэробных патогенных бактерий.
К диоксидину чувствительны клинические штаммы бактерий с полирезистентностью к антибиотикам. Препарат используется для промывания и тампонирования гнойных ран, а также может вводиться внутривенно, внутриартериально, интратрахеально через катетер или ингаляционно, внутриплеврально, в брюшную полость через ирригаторы.
Наш 20-летний опыт применения диоксидина в комплексном лечении больных с сепсисом, перитонитом, медиастинитом, с развернутой клиникой интоксикации, прогрессирующей полиорганной недостаточностью не подтверждает мнение некоторых специалистов о высокой токсичности этого препарата. Строгое соблюдение правил введения, разовых, суточных и курсовых доз позволяет избежать таких нежелательных побочных явлений, как тошнота, рвота или судороги.
0,1%-ный фурагин (солафур) — антимикробное средство из группы нитрофуранов. Препарат преимущественно действует на грамположительную микрофлору. Его МПК в 10-20 раз ниже, чем у фурациллина. Используется либо внутривенно при тяжелых формах течения раневой инфекции, при инфекционном процессе в легких, органах мочевыводящих путей, либо местно в виде 0,1%-ного раствора при лечении ран, инфицированных стафилококками, а также для промывания мочевого пузыря.
0,01%-ный мирамистин (миристамидопропилдиметилбензиламмоний хлорид) — новый антисептик из группы катионных ПАВ.
0,01%-ный водный раствор мирамистина с профилактической и лечебной целью используется в хирургии, травматологии и комбустиологии при незначительном количестве гнойного отделяемого в ране. Препаратом орошают поверхность ран и ожогов, рыхло тампонируют раны и свищевые ходы, марлевыми тампонами, смоченными антисептиком, промывают брюшную полость, вводят в плевральную полость и мочевой пузырь.
При обильной гнойной экссудации использование марлевых тампонов с растворами антисептиков для местного лечения ран неоправданно, так как тампоны, помещаемые в рану, быстро высыхают и, следовательно, не обладают необходимой для удаления гноя длительной осмотической активностью. В крайнем случае, рана может заполняться комбинированным тампоном — в центр марлевого тампона помещается силиконовая трубка, через которую 2-3 раза в сутки шприцем в рану вводится антисептик по 10-20 мл. Вместо 10%-ного раствора хлорида натрия для тампонирования послеоперационных ран в настоящее время используются современные мази на водорастворимой основе, высокую клиническую значимость которых можно считать доказанной.
Возможности использования мазей
К сожалению, до сих пор в ряде клиник используются мази на жировой основе с антибиотиками: линимент синтомицина, тетрациклиновая, эритромициновая и др. Однако мази на жировой основе с антибиотиками оказывают только кратковременное действие, поскольку вазелин-ланолиновая основа нарушает отток раневого отделяемого, не обеспечивает достаточного высвобождения активного ингредиента из композиции, не способствует проникновению антибиотика в глубь тканей, где находятся микробы, что приводит к переходу острых воспалительных заболеваний в хронические. Ввиду формирования в стационарах высокорезистентных штаммов микроорганизмов практически полностью утратили свою клиническую значимость и ихтиоловая мазь, и мазь Вишневского.
В последние годы в клиническую практику лечения гнойных ран в первой фазе раневого процесса внедрены новые мази — на полиэтиленоксидной основе (комбинации полиэтиленоксидов с молекулярным весом 400 и 1500).
Полиэтиленоксиды являются производными окиси этилена и обладают низкой токсичностью и выраженными осмотическими свойствами. При создании препаратов для лечения гнойных ран чаще всего используются полиэтиленоксид с молекулярным весом 400 (ПЭО-400) и полиэтиленоксид с молекулярным весом 1500 (ПЭО-1500).
В гнойной ране ПЭГ-1500 активно связывает воспалительный экссудат, отдавая его в повязку, с которой жидкость испаряется, а освободившиеся молекулы ПЭГ-1500 вновь присоединяют к себе экссудат, накапливающийся на дне раны.
Более мелкие молекулы (ПЭГ- 400) способны проникать в глубь тканей. Образуя с антибиотиком комплекс, ПЭГ-400 проводит его в ткани раны, где локализуются микробы. Этим он принципиально отличается от мазей на ланолин-вазелиновой основе, которые способны оказывать антимикробное действие только кратковременно и только на поверхности раны.
В состав современных мазей на полиэтиленоксидной основе введены различные антимикробные препараты:
Кроме того, в состав мазей введены такие препараты, как тримекаин, имеющий обезболивающий эффект, и метилурацил, обладающий анаболической и антикатаболической активностью, в целях стимуляции процессов клеточной регенерации.
Все мази на основе ПЭО отличаются от традиционных препаратов прежде всего многонаправленностью действия — осмотический эффект наблюдается до 18 часов, что позволяет делать перевязки только один раз в сутки, в то время как при использовании 10%-ного хлорида натрия повторные перевязки необходимо выполнять через каждые 3-4 часа, в противном случае повязка, пропитанная раствором и раневым отделяемым, полностью теряет осмотическую способность.
Еще одно преимущество мазей на полиэтиленоксидной основе — это широкий спектр антимикробной активности.
Причем по эффективности воздействия в силу однотипности мазевой основы все мази практически равноценны. При создании новых мазей особое внимание уделялось их антибактериальной активности. А. В. Вишневский по этому поводу писал: «Мы интересуемся силой, степенью бактерицидных свойств мази, ибо снизить, сбить, уничтожить инфекцию в ране всегда является задачей необходимой и благодарной» (Вишневский А. В., 1937).
Антимикробная активность новых мазей в отношении S.aureus находится на уровне 86-97,3%, Е. coil — 71-97%, Р.aeruginosa — 64-90,8%, Proteus spp. — 76-100%.
Для подавления в ранах грамотрицательных бактерий, в частности синегнойной палочки, широко применяется 10%-ная мазь мафенида-ацетата на гидрофильной основе.
Несмотря на интенсивное применение мазей, содержащих левомицетин или диоксидин, их высокая антимикробная активность сохраняется на протяжении более 20 лет, что указывает на слабый процесс нарастания резистентности госпитальных штаммов.
С внедрением полиэтиленгликолевой основы в технологию создания новых лекарственных форм появилась возможность создать мази с нитрофурановыми соединениями. На их основе выпускаются две мази: 0,5%-ная мазь хинифурила, а также фурагель, где в качестве основы использован сополимер акриловой кислоты (СОКАП) и ПЭГ-400.
Новые отечественные мази, содержащие нитрофурановые соединения, показывают высокую клиническую и бактериологическую эффективность. Так, фурагель более активен (94%) при наличии в ране S.aureus и менее активен (79%) при Р.aeruginosa. Maзь хинифурила одинаково высоко активна при наличии в ране грамположительной и грамотрицательной микрофлоры (87-88%). Оба препарата хорошо переносятся даже в случае их длительного использования при лечении трофических язв. Применение сополимера акриловой кислоты с полиэтиленгликолем в различных весовых соотношениях в качестве мазевой основы позволяет регулировать осмотическую активность мази как в сторону ее повышения, так и снижения, что очень важно при переходе раневого процесса во вторую фазу и необходимости продолжения лечения раны под повязкой.
Клиническая эффективность 1%-ной йодопироновой мази и многокомпонентной йодсодержащей мази (йодметриксилена) в качестве лечебного средства составляет 92,6-93,4%. Бактериологическая активность этих двух препаратов была одинаково высокой (91,8-92,6%) в отношении всех основных возбудителей острых гнойных процессов мягких тканей. Побочные эффекты (клинически значимые) наблюдались в 0,7% случаев и клинически незначимые — в 2,3% случаев. Следует особо подчеркнуть высокую эффективность этих препаратов при лечении ран с грибковым поражением, что часто наблюдается у больных ослабленных, с обширными ожоговыми ранами, трофическими язвами, пролежнями.
В настоящее время в клиническую практику внедрены только зарубежные йодсодержащие мази (повидон-йод и бетадин), хотя отечественный аналог был разработан более десяти лет назад.
Установлено, что уровень обсемененности ран аэробной микрофлорой при лечении мазями на ПЭГ-основе опускается «ниже критического» к 3-5-м суткам. Появление грануляций в среднем достигается к 4-м суткам, начало эпителизации — к 5-м.
Широкий спектр антимикробной активности мазей на полиэтиленгликолевой основе, их высокая и длительная осмотическая активность позволяют более чем в 80% случаев в течение 4-5 суток купировать острый гнойный процесс и закончить лечение неосложненных гнойных ран мягких тканей наложением первично-отсроченных швов, тогда как при использовании гипертонического раствора хлорида натрия в 90% случаев только в конце 2-3-й недели лечения под прикрытием системной антибактериальной терапии удается закрыть рану путем наложения вторичных швов.
Для лечения неспорогенной анаэробной инфекции наряду с диоксидином перспективные возможности открылись после изучения препарата нитазола, показавшего высокое антибактериальное действие на стафилококки, стрептококки, кишечную палочку, аэробные спорообразующие бактерии, патогенные анаэробные микроорганизмы как клостридиальные, так и неклостридиальные в виде монокультур и микробных ассоциаций. По спектру антибактериального действия нитазол имеет преимущества перед метронидазолом, к которому нечувствительны стафилококки, кишечная палочка, стрептококки. Нитазол оказывает противовоспалительное действие, являясь нестероидным противовоспалительным средством.
На основе нитазола были созданы пенообразующий аэрозоль «Нитазол» и две многокомпонентные мази «Стрептонитол» и «Нитацид». По антимикробной активности стрептонитол и нитацид значительно превосходят зарубежный препарат «Клион» (Венгрия), в состав которого входит метронидазол. Осмотическая активность стрептонитола гораздо ниже, чем у нитацида, что обусловлено введением в его состав вазелинового масла с водой. И стрептонитол, и нитацид, созданные для лечения ран с неклостридиальной анаэробной инфекцией, обладают равнозначным широким спектром антимикробной активности как в отношении грамположительной, так и грамотрицательной микрофлоры (84,2-88,5%). Обращает на себя внимание высокая активность этих препаратов при наличии в ране Р.aeruginosa (86,3-91,1%). Обе позиции показывают хорошую клиническую эффективность при наличии в ране анаэробной инфекции (88-89%).
Различие в осмотической активности позволяет использовать эти препараты ступенчато — сначала нитацид (с высокой осмотической активностью), затем стрептонитол.
Специалисты, занимающиеся лечением гнойных ран, хорошо знают, что бывают ситуации, когда одного скальпеля для полного удаления некротических тканей недостаточно: необходимы протеолитические препараты.
В настоящее время доказана высокая клиническая эффективность комплексного ферментного препарата «Протогентин», содержащего фермент природного происхождения «протеаза С» с протеолитическим действием, антибиотики (гентамицин и эритромицин), консерванты.
Мазевая основа препарата состоит из полиэтиленоксида с вазелиновым маслом. Умеренная осмотическая активность обеспечивает удаление из раны гноя.
Протогентин, наиболее активный в отношении P.aeruginosa и Е.coli, подавляет рост 83,4-90,4% штаммов.
Антимикробные компоненты мази «Протогентин» хорошо проникают под струп раны, вследствие чего в тканях раны создаются концентрации, намного превышающие МПК.
Достаточная осмотическая активность, широкий спектр антимикробной активности, хорошие фармакокинетические свойства протогентина способствуют сокращению сроков некролизиса. Мазевая основа не повреждает грануляционную ткань, что позволяет использовать этот препарат в течение длительного времени, пока требуется ферментативная очистка раневой поверхности.
После очищения раны от гнойно-некротического содержимого и достижения ее бактериологической санации наступает вторая фаза раневого процесса. Этот период характеризуется появлением в ране островков грануляционной ткани, которая, развиваясь, покрывает раневую поверхность полностью. Здоровая грануляционная ткань всегда яркая, сочная, легко кровоточит. При малейшем ухудшении процессов биосинтеза в ране изменяется внешний вид грануляций: они теряют яркую окраску, становятся мелкими, покрываются слизистым налетом. Одной из причин такого осложнения считается суперинфекция. Всякое замедление развития грануляций ведет к задержке и остановке процесса эпителизации.
Большое значение для скорейшего заживления ран во второй фазе имеет способность препаратов, используемых для местного лечения, оказывать бактерицидное действие в целях предупреждения вторичной инфекции, защитить грануляционную ткань от механических повреждений, а также оказывать умеренное влагопоглощающее действие и стимулировать рост грануляций.
Оптимальный вариант — сочетание этих факторов в одном препарате. К таким препаратам относятся современные комбинированные мази на регулируемой осмотической основе: метилдиоксилин, стрептонитол, а также пенные аэрозоли «Cульйодовизоль», «Гипозоль-АН», раневые покрытия на основе натриево-кальциевой соли альгиновой кислоты, масла, аэрозоли, гидроколлоидные покрытия (табл. 3).
Мазь «Метилдиоксилин» — многокомпонентная мазь, содержит диоксидин, метилурацил и гидрофобную эмульсионную основу с наличием касторового масла. Композиция винилина с эмульгатором и ПЭГ-400 в качестве основы мази позволила снизить осмотическую активность этого препарата до такого уровня, чтобы новая мазь не пересушивала молодую грануляционную ткань.
Мазь «Стрептонитол» содержит антибактериальные вещества стрептоцид и нитазол на гидрофильной эмульсионной основе, которая оказывает слабое осмотическое действие, удаляя избыток влаги, и одновременно защищает грануляционную ткань от механических повреждений. Препарат показан для лечения во второй фазе воспаления ранее инфицированных анаэробной, грамположительной и грамотрицательной микрофлорой ран при наличии ярких сочных грануляций.
Аэрозоли
На переходном этапе первой фазы раневого процесса во вторую высокую клиническую эффективность показывают современные пено- и пленкообразующие аэрозоли. Пенные препараты в аэрозольной упаковке перспективны для профилактики и лечения гнойных осложнений. Это обусловлено тем, что пены создают барьер для инфицирования ран, они не обладают «парниковым эффектом»; небольшим количеством препарата в составе пены можно покрывать большие по площади раневые поверхности и заполнять объемные раневые каналы и «карманы». Преимуществом аэрозольной формы является быстрота обработки, что важно при массовом поступлении пострадавших. Аппликации пен атравматичны.
В настоящее время создан ряд пенных препаратов:
В состав современных пенных препаратов обязательно входит какое-нибудь антимикробное средство, действующее на аэробную или на анаэробную микрофлору, включая неклостридиальную (бактероиды, пептококки, пептострептококки). Чаще всего используются диоксидин, йодовидон, циминаль и нитазол. Исследования антибактериальных свойств этих препаратов на моделях гнойных ран, вызванных анаэробной инфекцией, показывают выраженный терапевтический эффект, заключающийся в снижении высеваемости бактерий из ран к 3-5-му дню лечения до 10 1-2 микробов на 1 г ткани, уменьшении отечности и гиперемии, прекращении гнойной экссудации и в дальнейшем в заживлении ран.
Цимезоль кроме антисептика циминаля содержит анестетик тримекаин и гемостатик — порошок окисленной целлюлозы. Антисептическое действие циминаля усиливается благодаря сочетанию с димексидом и 1,2-пропилен-гликолем, которые обеспечивают проникновение циминаля в зоны некрозов и умеренный осмотический эффект.
Диоксизоль приготовлен на высокоосмотичной основе, а дегидратирующее действие диоксипласта сведено до минимума. Это определяет их применение соответственно в первой и во второй фазах раневого процесса при отсутствии в ранах большого количества гнойного отделяемого. Изучение антимикробной активности нового аэрозоля-диоксизоля показало преимущество этого препарата в случае выявления в ранах грамотрицательной микрофлоры. Диоксизоль подавляет Ps.aeruginosa в 92,5%.
Сульйодовизоль — пенообразующий аэрозольный препарат, расширяет возможности лечения ран йодовидоном в хирургии. Препарат показан для лечения ран во второй фазе раневого процесса, ранее инфицированных грамположительной и грамотрицательной аэробной микрофлорой.
Широкие клинические исследования показали необходимость использования пенообразующих аэрозолей только при отсутствии выраженного гнойно-воспалительного процесса на этапах подготовки раны к ее закрытию швами или методом пластики.
Масла
В настоящее время для лечения ран широко используются различные масла, в том числе и растительного происхождения (масло облепихи, масло шиповника, просяное масло — милиацил). Первые публикации о применении с этой целью различных масел относятся к эпохе Возрождения (Джованни де Виго, 1460-1520, Ambroslse Pare, 1510-1590).
Сравнительные экспериментальные исследования показали, что просяное масло прежде всего обладает более широким антимикробным спектром действия по сравнению с маслом шиповника или облепихи.
Просяное масло (милиацил) имеет высокое кислотное число (151,5-178,3), обусловленное большим содержанием свободных, ненасыщенных жирных кислот (олеиновой, линолевой, линоленовой). Этим объясняются стерильность препарата и его достаточный антимикробный эффект. Кроме того, входящее в состав просяного масла сложное стероидное соединение — пентациклический тритерпеноид — милиацин — обладает анаболическим действием и является стабилизатором мембран. Стабилизируя лизосомальные мембраны, милиацин предохраняет их от действия мембраноповреждающих факторов, например токсинов. В связи с этим уменьшается активность катепсинов, кислых РНК-азы и ДНК-азы, что приводит к уменьшению экссудации ткани, гипоксии, деполяризации РНК и ДНК.
Раневые покрытия
Широкие возможности в местном медикаментозном лечении ран открылись с появлением различных раневых покрытий, обладающих такими ценными качествами, как антимикробная активность, способность надежно предупреждать реинфицирование раневой поверхности, способность обеспечивать локальный гемостаз, ускорять образование грануляций, эпидермиса и активно поглощать раневой экссудат. Кроме того, современные раневые покрытия активно стимулируют образование грануляций и эпидермиса. При смене повязок эти препараты не вызывают болезненных ощущений. При длительном нахождении раневых покрытий на ране не возникает неприятного запаха.
В целях стимуляции процессов регенерации в ране наиболее широко используются перевязочные средства на основе производных белков и полисахаридов. С учетом специфического воздействия коллагеновых соединений на репаративные процессы в ране, а также данных по эффективности полисахаридных соединений с позиций создания оптимальных условий для формирования грануляционной ткани и миграции эпителиальных клеток разработаны раневые покрытия на основе белково-полисахаридных комплексов и их композиций с лекарственными препаратами. В качестве полисахаридных соединений использованы растительный полисахарид (альгинат натрия) и полисахарид животного происхождения (хитозан).
Биологически активные стимулирующие раневые покрытия
Биологически активные стимулирующие раневые покрытия с антимикробным и местно-анестезирующим действием выпускаются в четырех вариантах:
Перечисленные раневые покрытия благотворно влияют на течение регенераторных процессов в ране. Коллаген-альгинатные покрытия стимулируют рост грануляционной ткани, а коллаген-хитозановые — рост эпителиальных клеток.
В последние годы наибольшее распространение получили препараты на основе альгиновой кислоты и коллагена.
На основе смешанного натриево-кальциевой альгиновой кислоты созданы полифункциональные влагопоглощающие препараты для местного лечения ран во второй фазе (альгипор, альгимаф).
Стимулирующие раневые покрытия хорошо моделируются на различных участках тела, обеспечивают нормальный парообмен в ране, сорбируют избыток раневого экссудата, обладают пролонгированным антимикробным и обезболивающим действием, создают влажную среду, оптимальную для миграции эпителиальных клеток. Выход лекарственных средств из стимулирующих раневых покрытий осуществляется в течение 48-72 часов в зависимости от количества раневого экссудата в ране.
Все современные раневые покрытия обладают высокой антимикробной активностью за счет введенных в них противомикробных компонентов (сизомицин — в сипролине, мафенид-ацетат — в альгимафе, фурагин — в альгиколе АКФ и коллахите ФА).
Сравнительная оценка антибактериальной активности этих препаратов показывает, что элиминация S.aureus, Proteus spp. из ран быстрее происходит при использовании альгимафа и сипролина.
Гидроколлоиды
В последние годы за рубежом для лечения больных с длительно незаживающими ранами, трофическими язвами, пролежнями нашли применение гидроколлоидные лекарственные средства, в частности содержащие пектин — дуодерм (США), варигесив (США).
В НПО «Биотехнология» (Россия) совместно с Институтом хирургии им. А. В. Вишневского РАМН разработаны две гидроколлоидные лекарственные формы нового поколения на основе пектина: галактон — жидкий гидроколлоид, предназначенный для лечения длительно незаживающих глубоких ран мягких тканей с умеренным количеством гнойного отделяемого; галагран — сухой гидроколлоид (порошок) для лечения поверхностных ран мягких тканей, пролежней, трофических язв.
За счет введенного в состав диоксидина гидроколлоиды показывают лучшую активность по сравнению с другими препаратами в отношении P.auruginosa.
При сравнении гидроколлоидов (галаграна и галактона) с сорбентами (дежизаном и дебризаном) выявляется более широкий спектр положительных свойств гидроколлоидов. Прежде всего, гидроколлоиды стимулируют процессы регенерации и эпителизации, предупреждают реинфицирование раневой поверхности, поддерживают влажную среду под повязкой. Показатель сорбционной способности галаграна невысок: по воде — 3,56 г/г, по крови — 2,57 г/г; при этом верхний слой галаграна не смачивается модельными жидкостями на протяжении всего срока наблюдения (одни сутки).
Основное поглощение воды идет в течение 5 часов, далее наблюдается снижение количества сорбированной жидкости за счет подсыхания верхнего слоя и образования корочки, затрудняющей процесс дренирования. Частицы галаграна в контактном слое набухают, превращаясь в гелеобразную массу, которая равномерно растекается по ране.
По данным цитологического исследования, в первые трое суток использования галаграна в раневых отпечатках выявляется тенденция интенсивного формирования грануляционной ткани.
Учитывая природу биополимера, гидроколлоиды (галагран и галактон) целесообразно применять на стадии развития в ране репаративных процессов.
Гентацикол
Высокоэффективным препаратом для лечения длительно незаживающих ран, трофических язв, остеомиелита, диабетической стопы является препарат гентацикол — пролонгированная форма гентамицина на биодеградируемой (коллагеновой) основе.
Содержание антибиотика в биоптатах ран, получаемых от больных различных клинических групп, зависит от количества раневого отделяемого и скорости рассасывания коллагеновой основы.
Длительные и высокие концентрации гентамицина обнаруживаются при использовании гентацикола в лечении остеомиелита или в случаях окончательного закрытия швами остеомиелитической полости.
Гентацикол создает высокие концентрации гентамицина в тканях раны на протяжении 2 недель, причем эти концентрации намного превышают МПК основных возбудителей хирургической инфекции.
Биодеградируемая коллагеновая губка с гентамицином способствует купированию инфекционного процесса, активизирует пролиферацию всех клеточных элементов грануляционной ткани, усиливает коллагеногенез. Препарат может использоваться в ургентной хирургии в качестве местного гемостатика. Использование гентацикола в комплексном лечении различных ран позволяет сократить показания к проведению общей антибактериальной терапии с 16,6 до 5,5%; при этом в 98,2% случаев ранние реконструктивно-восстановительные кожно-пластические операции оказываются успешными.