что сильнее левофлоксацин или цефепим
Врач рассказал, как защититься от бактериальной пневмонии при коронавирусе
Разбираемся, что реально помогает и нужно ли при Covid-19 сразу пить антибиотики
Считается, что главная угроза при коронавирусе это поражение легких. Каким образом происходит ковидное поражение, в какой момент процесс осложняется бактериальной пневмонией? Как отличить одно от другого, есть ли способ защитить себя заранее и не допустить перехода COVID-19 в пневмонию, kp.ru рассказал кандидат медицинских наук, врач-пульмонолог Сеченовского университета Владимир Бекетов.
Первое, что важно уяснить, говорит эксперт, это то, что новая коронавирусная инфекция – это инфекция вирусная и входит в группу острых респираторных вирусных инфекций. Особняком в этой группе стоит только грипп. А значит, что для COVID-19, как и для всех респираторных вирусных инфекций, поражающих верхние дыхательные пути и легкие, характерен следующий феномен. Иммунная защита в легких ослабевает. Поэтому становится возможным присоединение вторичной бактериальной супер-инфекции примерно на 5 – 9 день течения любого острого респираторного вирусного заболевания.
РИСКИ ВОЗНИКНОВЕНИЯ ПНЕВМОНИИ
Риск присоединения бактериальной инфекции при заболевании COVID-19 увеличивается, если пациент попадает в стационар и при этом имеет хроническую патологию верхних и нижних дыхательных путей (например, ХОБЛ – хроническая обструктивная болезнь легких) или сердечную недостаточность.
КАК РАЗВИВАЕТСЯ ПНЕВМОНИЯ
В условиях, сниженной дыхательной и двигательной активности, когда слизь по бронхам движется меньше, на фоне интоксикации организма и снижения иммунитета, бактерии из носоглотки спускаются в нижние отделы дыхательного тракта и могут начать там размножаться.
Таким образом, может быть вызван сначала бактериальный бронхит, потом и бронхопневмония с переходом в пневмонию. Развитию бактериальной пневмонии может способствовать и длительное нахождение пациента на аппарате ИВЛ. Не смотря на соблюдение всех строжайших мер обеззараживания аппараты ИВЛ являются факторами риска возникновения вентилятор-ассоциированных пневмоний.
ДЕЙСТВИТЕЛЬНО ЛИ ПНЕВМОНИЯ ИДЕТ СЛЕДОМ ЗА COVID-19
По словам эксперта, на сегодняшний день ряд авторитетных медицинских ассоциаций выпустили меморандумы и открытые письма с призывами к коллегам уменьшить применение антибиотиков в ходе лечения COVID-19, потому что антибиотики не дают пользы, но приносят в данном случае вред, вплоть до токсического поражения печени и развития антибиотико-ассоциированной диареи.
Сам феномен вторичной бактериальной пневмонии при коронавирусе переоценен, продолжает эксперт. Подобные процессы развиваются в основном у пациентов с сердечной недостаточностью, а для них действуют меры повышенной предосторожности, ограничения в передвижении, рекомендации по самоизоляции и лечению на дому.
ВАЖНО!
Как обезопасить себя от пневмонии?
1. Вакцинироваться от пневмококка
Самая частая причина внебольничной пневмонии – это пневмококковая инфекция. Вакцинация от пневмококка дает иммунитет на 5 – 10 лет, если вы провакцинировались 13-валентной вакциной, то она гарантирует пожизненный иммунитет. Стафилококк, стрептококк и гемофильная палочка – эти бактерии чаще всего являются причинами вторичных бактериальных пневмоний.
2. Увлажнять воздух
Увлажнение воздуха в помещении достоверно снижает риски возникновения в бронхах слизистых гнойных пробок, которые ведут к закупориванию бронхов, к образованию в бронхах сухой мокроты и развитию там инфекции. Поэтому, если влажность воздуха будет выше 40%, то есть шансы на то, что бактериальная пневмония развиваться не будет. Важно понимать, что бытовые увлажнители воздуха нужно вовремя чистить.
НОВЫЕ ФТОРХИНОЛОНЫ: новые возможности лечения внебольничной пневмонии
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетлив
Инфекции дыхательных путей по частоте возникновения занимают первое место среди инфекционных заболеваний человека. Несмотря на наличие в арсенале врача большого количества антибактериальных препаратов разных классов, в последние годы наблюдается отчетливая тенденция к увеличению смертности от пневмонии во всех развитых странах мира. Причина может быть связана прежде всего с ростом резистентности основных возбудителей внебольничных инфекций дыхательных путей ко многим антибактериальным препаратам. Этим объясняется интерес клиницистов к новым антибактериальным средствам, к которым отмечается меньший уровень резистентности бактерий.
Этиология внебольничной пневмонии непосредственно связана с нормальной микрофлорой «нестерильных» верхних отделов дыхательных путей (полости рта, носа, рото- и носоглотки). Из множества видов микроорганизмов, колонизующих верхние отделы дыхательных путей, лишь некоторые, обладающие повышенной вирулентностью, проникая в нижние дыхательные пути, способны вызывать воспалительную реакцию даже при минимальных нарушениях защитных механизмов. Такими типичными бактериальными возбудителями внебольничной пневмонии являются следующие перечисленные ниже микроорганизмы.
Streptococcus pneumoniae — самый частый возбудитель внебольничной пневмонии у лиц всех возрастных групп (30-50%). Наиболее остро в настоящее время стоит проблема распространения среди пневмококков пенициллинрезистентных штаммов. В некоторых странах частота устойчивости пневмококков к пенициллину может достигать 60%. Масштабных исследований распространения резистентности пневмококков к пенициллину в нашей стране не проводилось. По данным локальных исследований в Москве, частота устойчивых штаммов составляет 2%, штаммов с промежуточной чувствительностью — около 20%. Устойчивость пневмококков к пенициллину связана не с продукцией β-лактамаз, а с модификацией мишени действия антибиотика в микробной клетке — пенициллинсвязывающих белков, поэтому ингибитор-защищенные пенициллины в отношении этих пневмококков также неактивны. Устойчивость пневмококков к пенициллину обычно ассоциируется с устойчивостью к цефалоспоринам I-II поколений, макролидам, тетрациклинам, ко-тримоксазолу.
Haemophilus influenzae — второй по частоте возбудитель (10-20%), особенно у лиц, страдающих хроническими обструктивными болезнями легких, а также у курильщиков; высокой природной активностью в отношении гемофильной палочки обладают аминопенициллины, амоксициллин/клавуланат, цефалоспорины II-IV поколений, карбапенемы, фторхинолоны. Основной механизм резистентности H. influenzae связан с продукцией β-лактамаз.
Staphylococcus aureus — нечастый возбудитель пневмонии (около 5%), наиболее опасен для пожилых людей, наркоманов, алкоголиков, после перенесенного гриппа. Препаратами выбора при стафилококковых пневмониях являются оксациллин, также активны амоксициллин/клавуланат, цефалоспорины, фторхинолоны.
Klebsiella pneumoniae — редкий возбудитель внебольничной пневмонии (менее 5%), встречается, как правило, у больных с тяжелыми сопутствующими заболеваниями (сахарный диабет, застойная сердечная недостаточность, цирроз печени и др.). Наиболее высокой природной активностью в отношении этого возбудителя обладают цефалоспорины III-IV поколений, карбапенемы, фторхинолоны.
Определенное значение в этиологии пневмонии имеют также два других микроорганизма, характеризующихся особыми биологическими свойствами и внутриклеточной локализацией в макроорганизме — Micoplasma pneumoniae и Chlamidia pneumoniae. В отношении этих микроорганизмов клинически неэффективны все β-лактамные антибиотики. Наибольшей природной активностью обладают макролиды и тетрациклины, несколько менее активны ранние фторхинолоны.
В настоящее время в качестве основных средств стартовой терапии внебольничной пневмонии в амбулаторной практике обычно рекомендуются аминопенициллины (ампициллин, амоксициллин), защищенные аминопенициллины (амоксициллин/клавуланат), пероральные цефалоспорины II поколения (цефуроксим аксетил), макролиды (эритромицин, кларитромицин, рокситромицин, азитромицин, спирамицин, мидекамицин). При тяжелом течении пневмонии у госпитализированных больных целесообразно применение парентеральных цефалоспоринов III поколения или фторхинолонов. Клиническая эффективность всех указанных препаратов примерно одинакова, однако при лечении внебольничной пневмонии ни один из этих антибиотиков не может считаться идеальным.
Аминопенициллины характеризуются высокой природной активностью в отношении S. pneumoniae (амоксициллин более высокой, чем ампициллин), однако о проблемах, связанных с возрастающим распространением пенициллинрезистентных пневмококков, упоминалось выше. Имеются данные, что амоксициллин пока сохраняет клиническую эффективность в отношении штаммов пневмококка с промежуточной чувствительностью, а также в отношении устойчивых штаммов. Однако можно предположить снижение клинической эффективности амоксициллина при выделении штаммов пневмококка с высоким уровнем резистентности. Аминопенициллины неэффективны при пневмонии, вызванной S. aureus и K. pneumoniae.
Назначение амоксициллина/клавуланата и цефуроксима аксетила предусмотрено большинством международных и отечественных стандартов лечения внебольничной пневмонии ввиду высокой активности против пневмококков, гемофильной палочки, стафилококков. Однако в отношении пенициллинрезистентных пневмококков мы сталкиваемся с теми же проблемами, что и у аминопенициллинов.
Следует подчеркнуть, что все пенициллины и цефалоспорины неактивны в отношении микоплазм, а также хламидий, и поэтому клинически неэффективны при атипичных пневмониях.
Макролидные антибиотики проявляют высокую природную активность в отношении пневмококков, стафилококков, микоплазм, хламидий и низкую — в отношении гемофильной палочки. Однако в последние годы во всех регионах мира, в том числе и в нашей стране, отмечается неуклонная тенденция повышения устойчивости пневмококков к макролидам. Резистентность пневмококков обычно ассоциируется с неуспехом терапии макролидами. Следует отметить, что новые полусинтетические макролиды не имеют преимуществ перед эритромицином, когда речь идет об устойчивых штаммах пневмококков. В последние годы значение макролидов при внебольничной пневмонии пересматривается. По всей видимости, эти препараты могут быть рекомендованы только в случае нетяжелой пневмонии при подозрении на атипичную этиологию.
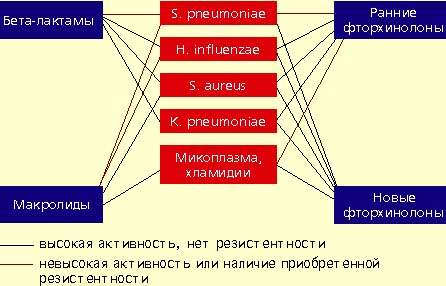 |
| Антимикробная активность бета-лактамов, макролидов и фторхинолонов в отношении наиболее значимых возбудителей внебольничной пневмонии |
Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей внебольничной пневмонии. Однако применение ранних фторхинолонов (ципрофлоксацин, офлоксацин, пефлоксацин) при внебольничной пневмонии было ограничено из-за их слабой природной активности в отношении основного возбудителя пневмонии — S. pneumoniae. Значения минимальных подавляющих концентраций (МПК) ранних фторхинолонов в отношении пневмококков составляют от 4 до 8 мкг/мл, а их концентрация в бронхолегочной ткани значительно ниже, что недостаточно для успешной терапии. Описаны случаи, когда терапия фторхинолонами при пневмококковой пневмонии не приносила успеха.
Определенные перспективы лечения внебольничной пневмонии связаны с появлением в последние годы препаратов нового поколения фторхинолонов, которые характеризуются более высокой активностью в отношении S. pneumoniae. Современная классификация фторхинолонов представлена в таблице.
Первым препаратом нового поколения фторхинолонов является левофлоксацин, представляющий собой левовращающий изомер офлоксацина. Левофлоксацин характеризуется более высокой активностью против пневмококков (МПК = 2 мкг/мл) по сравнению с офлоксацином и ципрофлоксацином, причем препарат сохраняет активность и в отношении пенициллинрезистентных штаммов S. pneumoniae. Левофлоксацин — это первый и пока единственный антибактериальный препарат, который официально рекомендован в США для лечения пневмонии, вызванной пенициллинрезистентными пневмококками. Среди новых фторхинолонов только левофлоксацин выпускается в двух лекарственных формах — для приема внутрь и для внутривенного введения. Поэтому левофлоксацин может применяться не только в амбулаторной практике, но и при тяжелых пневмониях у госпитализированных больных. В большом количестве клинических исследований показана высокая эффективность левофлоксацина при внебольничной пневмонии в дозе 500 мг, вводимой однократно в сутки. К несомненным достоинствам левофлоксацина можно отнести его хорошую переносимость.
Вторым препаратом нового поколения фторхинолонов, внедренным в клиническую практику, был спарфлоксацин. Он зарегистрирован в нашей стране и выпускается только в пероральной форме. Однако наряду с доказанной высокой клинической эффективностью следует отметить ряд нежелательных эффектов, отмеченных при его применении. Прежде всего речь идет о существенной фототоксичности спарфлоксацина (т. е. повышенной чувствительности кожи к ультрафиолету); по некоторым данным, частота возникновения этого нежелательного явления составляет более 10%. Фототоксичность характерна для всех препаратов класса фторхинолонов, однако при использовании других препаратов этой группы (например, левофлоксацина, офлоксацина, ципрофлоксацина) это побочное явление возникает гораздо реже. К другим достаточно серьезным нежелательным явлениям, связанным с приемом спарфлоксацина, относится удлинение интервала QT на ЭКГ, что может сопровождаться появлением желудочковых аритмий, иногда опасных для жизни. Клиническое значение этого феномена до конца не ясно, однако известен факт отзыва с рынка препарата этого класса (грепафлоксацина) именно по данной причине. Таким образом, спарфлоксацин, по всей видимости, не может быть рекомендован для рутинного применения в амбулаторной практике при пневмонии, учитывая наличие других, более безопасных препаратов этой группы.
Последним зарегистрированным в нашей стране новым фторхинолоном является моксифлоксацин. Пока он существует только для перорального приема, однако в следующем году ожидается появление в клинической практике парентеральной лекарственной формы. Моксифлоксацин характеризуется очень высокой природной активностью в отношении пневмококков (МПК = 0,25 мкг/мл), в том числе пенициллинрезистентных штаммов, а также более высокой активностью (по сравнению с ранними фторхинолонами) в отношении микоплазм и хламидий. Моксифлоксацин в суточной дозе 400 мг (однократно) показал высокую клиническую эффективность и хорошую переносимость при внебольничной пневмонии. В контролируемых исследованиях не отмечено клинически значимого удлинения интервала QT и существенной фототоксичности.
Ряд перспективных препаратов нового поколения фторхинолонов в настоящее время проходят стадию клинического изучения. В 2001 году ожидается разрешение клинического применения в России еще двух препаратов этой группы — гемифлоксацина и гатифлоксацина.
Цефепим : инструкция по применению
Состав
Описание
Фармакотерапевтическая группа
Фармакологические свойства
Применение у особых групп пациентов
Показания к применению
Противопоказания
Способ применения и дозы
Дозы и способ введения препарата зависят от чувствительности возбудителя, тяжести инфекции, функции почек и общего состояния пациента.
Рекомендации относительно дозирования лекарственного средства приведены в таблице 1.
Таблица 1. Дозирование у пациентов с нормальной функцией почек (клиренс креатинина (КК) более 50 мл/мин)
Локализация и тип инфекции Продолжитель-ность 2 (дни) Взрослые и дети старше 12 лет (с массой тела более 40 кг) Эмпирическая терапия пациентов с фебрильной нейтропенией Неосложненные или осложненные инфекции мочевых путей, включая пиелонефрит Тяжелые неосложнённые или осложненные инфекции мочевых путей, в том числе пиелонефрит Инфекции кожи и ее структур, вызываемые S. aureus или S.pyogens. Осложнённые интраабдоминальные инфекции (в сочетании с метронидазолом) Дети в возрасте от 1 месяца до 12 лет (с массой тела ≤ 40 кг): пневмония, осложнённые инфекции мочевыводящих путей. Очень тяжёлые инфекции: сепсис, бактериальный менингит, эмпирическое лечение эпизодов фебрильной нейтропении. 2 месяца – 12 лет (с массой тела ≤ 40 кг) 50 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 50 мг/кг массы тела каждые 8 часов 50 мг/кг массы тела каждые 8 часов Продолжительность: 10 дней 7-10 дней 30 мг/кг массы тела каждые 12 часов Серьёзные инфекции: 30 мг/кг массы тела каждые 8 часов 30 мг/кг массы тела каждые 8 часов Продолжительность: 10 дней 7-10 дней |
* В том числе случаи, связанные с одновременной бактериемией.
** Или до окончания нейтропении. У пациентов со снижением температуры, но нейтропенией более 7 дней, должна быть пересмотрена необходимость продолжения антибактериальной терапии.
*** Внутримышечный путь введения показан только для легкой и умеренной неосложненной или осложненной инфекции мочевыводящих путей, вызванной E. coli.
1 При лечении пневмонии, вызванной P. aeruginosa: 2 г вводить в/в каждые 8 часов.
2 Продолжительность лечения, как правило, составляет от 7 до 10 дней. Максимальная продолжительность в целом – не менее 7, но не более 14 дней. Продолжительность эмпирического лечения фебрильной нейтропении: от 7 дней до исчезновения нейтропении.
Опыт применения у детей в возрасте до 1 месяца ограничен и основывается на расчете доз, исходя из опыта применения дозы 50 мг/кг массы тела, полученной на основании фармакокинетических данных у пациентов старше 1 месяца, что соответствует дозе 30 мг/кг массы тела каждые 12 или 8 часов для детей в возрасте от 1 до 2 месяцев. Дети этого возраста должны тщательно контролироваться во время введения препарата.
У детей с массой тела более 40 кг рекомендуется доза, как для взрослых (смотрите таблицу). У детей старше 12 лет с массой тела менее 40 кг рекомендуется доза, как для детей с массой тела ≤ 40 кг. Максимальная доза у детей не должна превышать максимальную дозу для взрослых (2,0 г каждые 8 часов).
Продолжительность лечения, как правило, составляет от 7 до 10 дней. В целом цефепим рекомендуется применять не менее 7, но не более 14 дней.
При эмпирическом лечении фебрильной нейтропении продолжительность лечения обычно составляет до 7 дней или до окончания нейтропении.
Пациенты с нарушенной функцией почек. Цефепим выводится почками путем клубочковой фильтрации, поэтому больным с нарушениями функции почек (клиренс креатинина (КК) менее 50 мл/мин) дозу Цефепима необходимо откорректировать. У этих пациентов рекомендуемая начальная доза цефепима должна быть такой же, как у пациентов с КК более 50 мл/мин, за исключением пациентов, подвергающихся гемодиализу (таблица 2).
Таблица 2. Рекомендуемые дозы Цефепима для взрослых.
* В день проведения диализа инъекцию лекарственного средства необходимо выполнять после окончания процедуры диализа.
Если известна только концентрация креатинина в сыворотке крови, тогда КК можно определять по нижеуказанным формулам.
Мужчины: КК (мл/мин) = масса тела (кг)×(140 – возраст) : 72×креатинин плазмы крови (мг/дл).
Женщины: КК (мл/мин) = показатель у мужчин×0,85.
При гемодиализе за 3 ч удаляется приблизительно 68 % дозы препарата. При непрерывном амбулаторном перитонеальном диализе препарат можно применять в исходных рекомендованных дозах – 500 мг, 1 г или 2 г в зависимости от тяжести инфекции с интервалом 48 ч.
У детей при нарушении функции почек рекомендуются изменения режима дозирования, пропорциональные тем, которые принимаются у взрослых, в соответствии с приведённой ниже таблицей.
Расчет показателей КК у детей
КК (мл/мин/1,73 м 2 ) = 0,55×рост (см): креатинин плазмы крови (мг/дл) или
КК (мл/мин/1,73 м 2 ) = 0,52×рост (см): креатинин плазмы крови (мг/дл) −3,6.
Способ применения
Цефепим после восстановления вводят внутримышечно, внутривенно струйно медленно в течение 3-5 мин либо капельно путём инфузии в течение не менее 30 мин.
Приготовление раствора для внутривенного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
Восстановленный раствор разбавляют одним из следующих совместимых инфузионных растворов для внутривенного введения: 0,9 % раствор хлорида натрия; 5 % и 10 % раствор декстрозы; 5% раствор декстрозы с 0,9 % раствором хлорида натрия; 1/6 М раствор натрия лактата; раствор Рингера лактата; раствор Рингера лактата с 5 % раствором глюкозы.
Приготовление раствора для внутримышечного введения
Цефепим восстанавливают одним из следующих растворителей: стерильная вода для инъекций; 0,9 % раствор хлорида натрия для инъекций; 5 % раствор декстрозы для инъекций; стерильная бактериостатическая вода для инъекций с парабенами или бензиловым спиртом в количествах, указанных в таблице 3.
