Что такое ортоборная кислота
Ортоборная кислота: применение, свойства, польза
У каждого человека наверняка найдется в аптечке такое вещество, как ортоборная кислота. Многие используют ее в качестве косметического или лекарственного средства. Но крайне важно понимать, в чем же различие между борным спиртом и кислотой. Необходимо лучше разобраться в данной теме, чтобы избежать проблем со здоровьем и по назначению использовать каждое вещество.
Что же это?
Ортоборная кислота – это в первую очередь кристаллическое вещество, из которого в дальнейшем приготавливают раствор. Данное соединение является слабой кислотой. Химическая формула ортоборной кислоты: H3BO3. Данное соединение ограничено растворяется в холодной воде. Но растворимость ортоборной кислоты при нагревании увеличивается. Например, растворимость данного соединения при 0 градусов Цельсия составляет 2,66 г на 100 г воды, а при температуре 100 градусов Цельсия возможно растворить уже 39,7 г вещества.

И также растворимость ортоборной кислоты зависит от вида растворителя. Если это минеральные кислоты, то соединение плохо вступает с ними в реакцию, а, например, в растворах солей растворяется гораздо лучше. Ортоборную кислоту можно растворять в одноатомных и многоатомных спиртах. И также довольно хорошими растворителями для данного соединения являются ацетон и пиридин. Необходимо добавить, что ортоборная и борная кислота – разные названия одного и того же вещества.
Нахождение в природе
Ортоборная кислота в природе находится в минерале, который носит название «сассолин». Помимо этого, данное соединение было обнаружено в термальных водах. Получают ортоборную кислоту именно из них. Для этого проводят экстракцию с помощью спиртов. И также возможен и другой метод получения, например с помощью сорбентов неорганической и органической природы.
Ионная форма
Ортоборная кислота обладает слабыми электролитическими свойствами. Если воздействовать на раствор в воде с данных соединением электрическим током, то будет происходить электролитическая диссоциация на ионы. Уравнение данного процесса: H3BO3 ⇆ 3H+ + BO33-. В данном случае BO33- является кислотным остатком ортоборной кислоты. Благодаря такой диссоциации и наличию кислотного остатка кислота способна образовывать соли с основными соединениями.
Применение
Ортоборная кислота находит широкое применение в различных областях. В промышленности ее используют для получения боросиликатного стекла. Главной особенностью его является то, что оно проявляет большую устойчивость в условиях резкого изменения температуры.
И также данное соединение находит свое применение в получении различной лакокрасочной продукции, цемента, красителей, косметических средств, лекарств и т. д. Помимо этого, ортоборную кислоту применяют в качестве ингибитора коррозии, что необходимо на различных предприятиях. И также кислоту используют как удобрение для растений.
Данное соединение находит свое применение и в лабораторной практике: его используют для приготовления буферных растворов. Ортофосфорная кислота имеет частое применение при лечении, так как обладает антисептическими свойствами. Именно поэтому существуют различные формы выпуска кислоты. Помимо простого раствора, это могут быть мази, присыпки, кремы, различные пасты. Также кислота находит свое применение и в пищевой промышленности. Обнаружить ее можно по номеру Е284. Кислоту используют как консервирующее вещество.
Использование в медицинской практике
Ортоборная кислота используется при лечении различных заболеваний, главными ее преимуществами являются антисептические свойства. Вещество имеет несколько форм выпуска. Но каждый препарат, представленный в своем виде, необходимо использовать и хранить правильно. Например, порошкообразную форму необходимо готовить только перед применением.
Используют ортоборную кислоту для лечения конъюнктивита, в случаях, когда поражена инфекционными заболеваниями большая часть кожи, при воспалении ушей и слизистых оболочек.
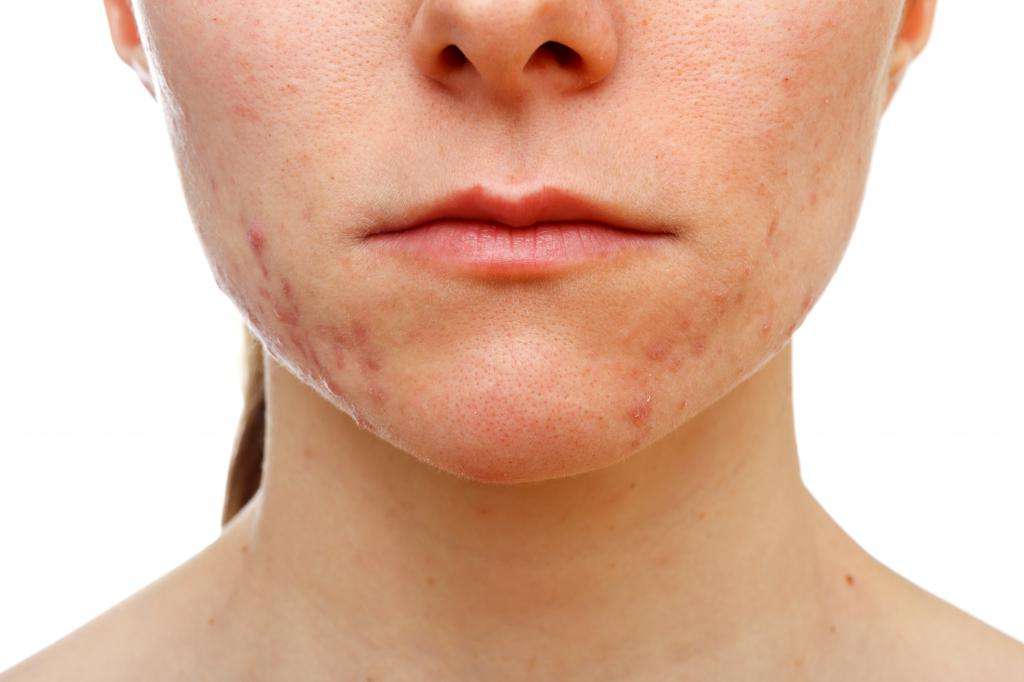
Применение при борьбе от прыщей
Ортоборная кислота – это отличный помощник при борьбе с прыщами. Тем более что цена на данное средство минимальная. Но прежде чем использовать данную кислоту в косметических целях, необходимо проконсультироваться со специалистом и убедиться, что нет чувствительности к компонентам раствора, чтобы в будущем не проявилась аллергическая реакция.
Для лечения угревой сыпи необходимо протирать пораженные участки кожи небольшим количеством ортоборной кислоты, используя ватный диск. И также можно точечно наносить кислоту при помощи ватной палочки. Данное средство отлично помогает справиться с нежелательными прыщами, так как оно немного подсушивает кожу, проявляет бактерицидные свойства и снимает сильное воспаление.
Использование в минеральной воде
Лечебные минеральные воды содержат огромное количество минеральных соединений, которые так нужны организму человека. Стоит отметить, что употреблять их следует либо исключительно в лечебных целях, либо нерегулярно для поддержания хорошего самочувствия.
Но прежде чем употреблять лечебные воды, обязательно необходимо проконсультироваться с соответствующими специалистами. Помимо таких веществ, как йод, железо, различные органические соединения, минеральные воды содержат и бор, который пересчитывают на борную кислоту. Ортоборная кислота в минеральных водах может содержаться в количествах от 35 до 60 мг на один литр воды.
Данное соединение находит широкое применение в жизни человека, но следует аккуратно с ним обращаться, чтобы оно шло исключительно на пользу здоровья.
Ортоборная кислота
Ортоборная кислота
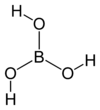
| Борная кислота | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Ортоборная кислота |
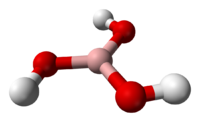
| Химическая формула | H3BO3 |
| Отн. молек. масса | 61,83 а. е. м. |
| Молярная масса | 61,83 г/моль |
| Физические свойства | |
| Плотность вещества | 1,435 (15 °C) г/см³ |
| Состояние (ст. усл.) | твёрдое |
| Термические свойства | |
| Температура плавления | 171 (разл.) °C |
| Химические свойства | |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | 5,74 (25 °C) г/100 мл |
| Классификация | |
| номер CAS | 10043-35-3 |
Бо́рная кислота́ (ортоборная кислота) 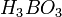
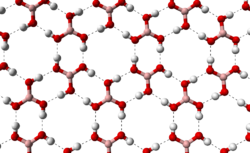
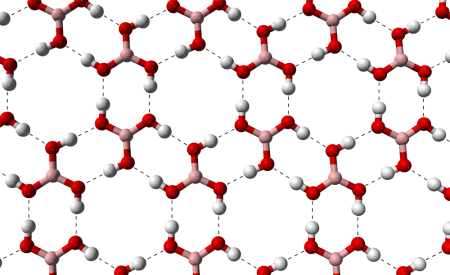
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решетку, в которой молекулы 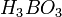
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту 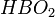
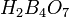
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n.
Содержание
Свойства
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Применение
Литература
Примечания
См. также
Полезное
Смотреть что такое «Ортоборная кислота» в других словарях:
ортоборная кислота — boro rūgštis statusas T sritis chemija formulė H₃BO₃ atitikmenys: angl. boric acid; orthoboric acid rus. ортоборная кислота ryšiai: sinonimas – ortoborato rūgštis sinonimas – vandenilio trioksoboratas (3–) … Chemijos terminų aiškinamasis žodynas
Борная кислота — ортоборная кислота, H3BO3, слабая неорганическая трехосновная кислота; бесцветные кристаллы в виде чешуек, плотность 1,48 г/см3. Умеренно растворима в холодной воде, лучше в горячей, чем пользуются для её очистки (растворимость в г на 100 … Большая советская энциклопедия
Борная кислота — ортоборная кислота, Н3ВO3 слабая неорганическая кислота; в свободном виде бесцветные кристаллы с плотностью 1480 кг/м3. Умеренно растворима в воде (2,66 г на 100 г воды при 0° С и 39,7 г при 100° С). Применяют: при модифицировании расплавленного… … Энциклопедический словарь по металлургии
БОРНАЯ КИСЛОТА — ортоборная кислота, Н3ВО3 слабая неорганическая кислота; в свободном виде бесцветные кристаллы с плотностью 1480 кг/м3. Умеренно растворима в воде (2,66 г на 100 г воды при 0° С и 39,7 г при 100° С). Применяют: при модифицировании… … Металлургический словарь
Борная кислота — Борная кислота … Википедия
Борная кислота — (ортоборная кислота) (H3BO3) получается или при кислотном разложении природных боратов, или при физико химической обработке неочищенной борной кислоты. Она существует в виде порошка или мелких чешуек, слюдистых хлопьев или стекловидных кусков с… … Официальная терминология
БОРНАЯ КИСЛОТА — ортоборная кисло т а, Н3ВО3 слабая неорганич. к та; в свободном виде бесцветные кристаллы с плотн. 1480 кг/м3. Умеренно растворима в воде, лучше в горячей (растворимость в г на 100 г H2O: 2,66 при 0 °С и 39,7 при 100 °С). Б. к. применяют в… … Большой энциклопедический политехнический словарь
Борные кислоты — Борная кислота Общие … Википедия
Е284 — Борная кислота Общие … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Борная кислота
Из Википедии — свободной энциклопедии
наименование

2,52 (0 °C)
4,72 (+20 °C)
5,74 (+25 °C)
19,10 (+80 °C)
27,53 (100 °C)
г/100 мл
Бо́рная кислота́ (ортоборная кислота или лат. acidum Boricum ) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
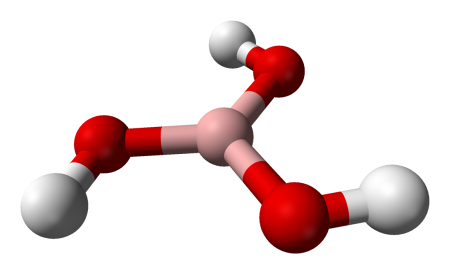
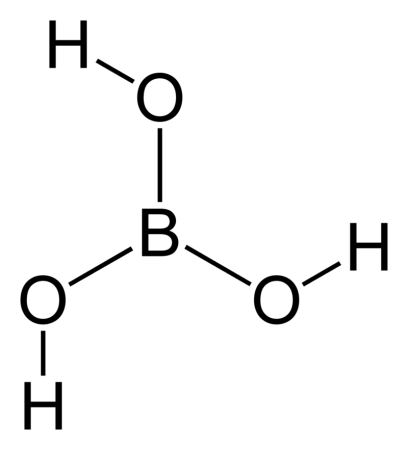
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272 пм. Расстояние между соседними слоями — 318 пм.
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-НВО2 с кубической решёткой, β-НВО2 с моноклинной решёткой и α-НВО2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы Н3m-2nВmО3m-n. В природе встречается в виде минерала сассолина.
Борная кислота
| Борная кислота | |
|---|---|
 | |
 | |
| Систематическое наименование | Ортоборная кислота |
| Хим. формула | H3BO3 |
| Состояние | твёрдое |
| Молярная масса | 61,83 г/моль |
| Плотность | 1,435 (15 °C) |
| Т. плав. | 170.9 °C, 444 K, 340 °F |
| Т. кип. | 300 °C, 573 K, 572 °F °C |
| pKa | 9,24 (I), 12,74 (II), 13,80 (III) |
| Растворимость в воде | |
| ГОСТ | ГОСТ 9656-75 ГОСТ 18704-78 |
| Рег. номер CAS | 10043-35-3 |
| PubChem | 7628 |
| Рег. номер EINECS | 233-139-2 |
| SMILES | |
| Кодекс Алиментариус | E284 |
| RTECS | ED4550000 |
| ChEBI | 33118 |
| ChemSpider | 7346 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Борная кислота (ортоборная кислота или лат. acidum Boricum ) — слабая, одноосновная кислота Льюиса, часто используемая в качестве инсектицида, антисептика, огнезащитного состава, поглотителя нейтронов или предшественника для получения иных химических составов. Имеет химическую формулу H3BO3 (или B(OH)3).
Бесцветное кристаллическое вещество в виде чешуек без запаха, имеет слоистую триклинную решётку, в которой молекулы кислоты соединены водородными связями в плоские слои, слои соединены между собой межмолекулярными связями, длина которых составляет 272 пм. Расстояние между соседними слоями — 318 пм.
Метаборная кислота (HBO2) также представляет собой бесцветные кристаллы. Она существует в трёх модификациях — наиболее устойчивой γ-HBO2 с кубической решёткой, β-HBO2 с моноклинной решёткой и α-HBO2 с ромбической решёткой.
При нагревании ортоборная кислота теряет воду и сначала переходит в метаборную кислоту, затем в тетраборную H2B4O7. При дальнейшем нагревании обезвоживается до борного ангидрида.
Водные растворы борной кислоты являются смесью полиборных кислот общей формулы H3m-2nВmO3m-n. В природе встречается в виде минерала сассолина.
Содержание
Нахождение в природе
В природе свободная борная кислота встречается в виде минерала сассолина, в горячих источниках и минеральных водах.
Получение
Борная кислота может быть получена путём смешения буры (Тетрабората натрия) с минеральной кислотой, например, соляной:
Также является продуктом гидролиза диборана или тригалогенидов бора:
B2H6 + 6H2O → 2H3BO3 + 6H2 BCl3 + 3H2O → H3BO3 + 3HCl 
Борная кислота ОСЧ
Свойства
Она легко вытесняется из растворов своих солей большинством других кислот. Соли её, называемые боратами, производятся обычно от различных полиборных кислот, чаще всего — тетраборной H2B4O7, которая является значительно более сильной кислотой, чем ортоборная.
Очень слабые признаки амфотерности B(OH)3 проявляет, образуя малоустойчивый гидросульфат бора В(HSO4)3.
Мета- и тетрабораты гидролизуются, но в меньшей степени (реакции, обратные приведённым).
В подкисленных водных растворах боратов устанавливаются следующие равновесия:
При нагревании борная кислота растворяет оксиды металлов, образуя соли.
Со спиртами в присутствии концентрированной серной кислоты образует эфиры:
Образование борнометилового эфира В(OCH3)3 является качественной реакцией на H3BO3 и соли борных кислот, при поджигании борнометиловый эфир горит красивым ярко-зеленым пламенем.
Борная кислота в медицине
Борный спирт (лат. Solutio Acidi borici spirituosa ) — раствор борной кислоты в этиловом спирте (как правило, в 70 % этаноле).
Спиртовые растворы борной кислоты в концентрации 0,5 %, 1 %, 2 %, 3 %, 5 % готовятся на 70 % этиловом спирте и применяются в качестве антисептика и как противозудное средство при обтирании здоровых участков кожи вокруг очагов пиодермии, а также в качестве ушных капель.
Борная кислота применяется в медицине с 60-х годов XIX века как антисептическое средство, не раздражающее ран и не имеющее вкуса, запаха и цвета. В современной медицине противомикробная эффективность борной кислоты считается низкой.
Использование борной кислоты в качестве антисептического средства для детей, а также беременных и кормящих женщин было запрещено 2 февраля 1987 года Министерством здравоохранения СССР по рекомендации Фармакологического комитета с формулировкой: «…запретить использование борной кислоты в качестве антисептического средства у детей грудного возраста, а также у женщин в период беременности и лактации в связи с её низкой активностью и высокой токсичностью».