Что такое острый эндотоксикоз
Что такое острый эндотоксикоз
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Клиника синдрома эндогенной интоксикации.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
Раздел: Патогенез и клиническая диагностика синдрома эндогенной интоксикации (В.В. Щекотов)
I. ПАТОГЕНЕЗ И КЛИНИЧЕСКАЯ ДИАГНОСТИКА СИНДРОМА ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
1. ОПРЕДЕЛЕНИЕ СИНДРОМА ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
ИНТОКСИКАЦИЯ (лат. in в, внутрь + греч. toxikon яд) – патологическое состояние, возникающее в результате действия на организм токсических (ядовитых) веществ эндогенного или экзогенного происхождения.
Соответственно различают экзогенные и эндогенные интоксикации (И). Понятие «интоксикация» нередко отождествляют с понятием «отравление», хотя отравлением принято называть только те И, которые вызваны экзогенными ядами.
Понятие «яды» охватывает по существу все токсические вещества окружающей среды, которые способны при определенных условиях вызвать И организма. Эндогенные И объединены термином «аутоинтоксикация». Впервые упоминание об И как причине болезни встречается у Парацельса, который различал болезни от внутренних и наружных ядов. Экспериментальное изучение И в России связано с работами Пеликана (1878), изучавшего патогенез И, вызванных некоторыми ядами, имеющими судебно-медицинское значение, и школы В. В. Пашутина; ученик В. В. Пашутина С. Бочаров (1884) показал роль продуктов гниения в патогенезе И при сепсисе.
Эндогенная интоксикация (ЭнИ) – это полиэтиологичный и полипатогенетичный синдром, характеризующийся накоплением в тканях и биологических жидкостях эндогенных токсических субстанций (ЭТС) – избытка продуктов нормального или извращенного обмена веществ или клеточного реагирования. Она представляет собой сложное многокомпонентное явление, включающее:
— источник токсемии, обеспечивающий образование ЭТС;
— биологические барьеры, предупреждающие прорыв эндогенных
токсинов за пределы источника;
— механизмы переноса этих токсических продуктов к клеткам-
мишеням, к органам биотрансформации и/или экскреции;
— механизмы иммобилизации и депонирования, биотрансформации
(нейтрализации) и экскреции токсических продуктов;
— эффекторные ответы на интоксикацию в виде так называемой
вторичной токсической агрессии, в результате которой ЭнИ в значительной мере теряет свою специфичность.
Хотя эндогенная интоксикация полиэтиологична, можно выделить следующие первичные механизмы ее развития:
— продукционный или обменный, обусловленный избыточной продукцией эндогенных токсических субстанций (разлитой перитонит, острый панкреатит, пневмония);
— резорбционный, когда происходит резорбция токсических веществ из ограниченного очага инфекции, распадающихся тканей (кишечная непроходимость, флегмоны мягких тканей, абсцессы и т. д.);
— реперфузионный, при котором в системный кровоток поступают вещества, накопившиеся в длительно ишемизированных тканях, а также выделившиеся из клеток этих тканей при их повреждении активным
кислородом и избытком свободных радикалов на фоне несостоятельности антиоксидантной защиты (шок, реперфузионный синдром, операции с применением аппарата искусственного
кровообращения и т.д.);
— ретенционный, при котором накопление ЭТС происходит в результате нарушения их выделения естественными органами детоксикации (острая почечная (ОПН) и печеночная (ОПечН)
недостаточность);
— инфекционный, в результате поступления микроорганизмов, продуктов их обмена и распада из очага инвазивной инфекции или путем транслокации из извращенно контаминированного желудочно-
кишечного тракта. В развитии острого эндотоксикоза одновременно или последовательно могут участвовать несколько механизмов образования ЭТС и накопления их во внутренней среде организма.
Вопрос о том, что может являться такими токсическими субстанциями и обусловливать тяжесть состояния пациентов, сложен и противоречив, так как многие вещества в зависимости от их концентрации могут оказывать и благоприятное, и неблагоприятное функциональное воздействие, а большинство из них вообще не идентифицированы. Можно классифицировать их в зависимости от этиологии и механизма выведения.
2.КЛАССИФИКАЦИЯ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
2.1. ПРИЧИНЫ И МЕХАНИЗМЫ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Эндогенная И может быть вызвана токсическими продуктами, образующимися в организме при различных заболеваниях (аллергических болезнях, ожоговой болезни) и экстремальных состояниях. К эндогенной И. относится отравление продуктами жизнедеятельности бактерий, находящихся в организме. В ряде случаев И. становится ведущим патогенетическим фактором, определяющим развитие клинической картины (уремия, токсикоинфекции, тиреотоксикоз, токсическая дифтерия, токсическая диспепсия и др).
В механизмах как эндогенной, так и экзогенной И. имеется много общего, т. к. в том и другом случае повреждающим фактором является токсический агент. Кроме того, И, вызванная экзогенным фактором, может реализоваться эндогенным путем; например, отравление антихолинэстеразными ядами типа физостигмина или фосфакола в основном сводится к аутоинтоксикации ацетилхолином, который накапливается в синаптических образованиях вследствие прекращения его ферментативного гидролиза.
К числу веществ, накапливающихся в организме при различных заболеваниях и вызывающих эндогенную И., относятся химические соединения различной природы: продукты превращения аминокислот (фенол, крезол, индол, скатол, путресцин, кадаверин), жиров (γ-оксимасляная кислота, ацетоуксусная кислота и ацетон). Имеют значение также активные белки, аденилнуклеотиды, гистамин, серотонин, кинины и другие физиологически активные вещества, выделяющиеся в значительных количествах при повреждении клеток и тканей. При инфекционных заболеваниях происходит накопление бактериальных токсинов и других продуктов жизнедеятельности микробов, а также продуктов распада тканей.
Основной причиной И в условиях трансплантации является реакция трансплантат против хозяина. При возникновении И в различных экстремальных состояниях, например, при ожоговой болезни, травме, патогенетическое значение имеет подавление детоксицирующей способности ретикулоэндотелиальной системы, в связи с чем в организме происходит накопление эндотоксина Е. coli. вызывающего расстройства микроциркуляции. Имеет место также стимулирование неферментативного перекисного окисления липидов клеточных мембран, в результате чего в организме накапливаются токсичные продукты, что вызывает изменение проницаемости этих мембран. При лучевом поражении, кроме того, происходит накопление липидных и хиноноподобных токсинов, повреждающее действие которых на клетки приводит к накоплению в организме гистамина и других физиологически активных продуктов белкового распада. Снижение содержания в тканях естественного ингибитора цепных окислительных реакций токоферола имеет значение для развития И при авитаминозе Е и новообразованиях.
2.2. ИСТОЧНИКИ ЭНДОТОКСИНЕМИИ
— продукты нормального обмена веществ в высоких концентрациях (лактат, пируват, мочевая кислота, мочевина, креатинин, билирубина глюкуронид и др.);
— вещества, избыточно образующиеся при извращенном метаболизме (кетоны, альдегиды, спирты, карбоновые кислоты, аммиак и др.);
— продукты распада клеток и тканей из очагов тканевой деструкции и/или из ЖКТ при нарушении барьерных функций мембран (липазы, лизосомальные ферменты, катионные белки, миоглобин, индол, скатол, фенол и др.);
-компоненты и эффекторы регуляторных систем организма в патологических концентрациях: активированные ферменты (лизосомальные, протеолитические, продукты активации калликреинкининового каскада, системы свертывания крови и фибринолиза);
— медиаторы воспаления, биогенные амины, цитокины, простагландины, лейкотриены, белки острой фазы и другие биологически активные вещества;
— активные соединения, образующиеся при перекисном окислении липидов;
— микробные токсины (экзо- и эндотоксины) и другие факторы патогенности микроорганизмов (патогенных, условно-патогенных, непатогенных);
— иммуночужеродные продукты клеточного распада, антигены и иммунные комплексы-агрессоры.
2.3. ПУТИ ЭЛИМИНАЦИИ ЭНДОГЕННЫХ ТОКСИНОВ
— газообразные вещества – выделяются через легкие;
— гидрофильные низко- и среднемолекулярные вещества – удаляются почками, через кожу, ЖКТ в виде растворов;
— гидрофобные низко- и среднемолекулярные вещества – транспортируются белками и/или клетками крови в печень и легкие, где и биотрансформируются при участии монооксигеназной системы или
претерпевают изменения в реакциях связывания с последующим удалением через почки, кожу, ЖКТ;
— гидрофобные низко- и среднемолекулярные вещества – связываются с белками плазмы крови, приобретают свойства гаптенов и поглощаются клетками иммунной системы;
— высокомолекулярные соединения – транспортируются по лимфатическим сосудам, элиминируются моноцитарно-макрофагальной системой (до 80% макрофагов организма находится в печени).
2.4. СТАДИИ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Острый эндотоксикоз протекает как каскадный процесс. Развитие и прогрессирование его связано с несоответствием между образованием (поступлением и т.д.) токсических субстанций, в том числе образующихся в результате последующей токсической аутоагрессии, и способностью органов, входящих в функциональную систему детоксикации (легкие, печень, почки, ЖКТ, кожа, система иммунологического надзора), их трансформировать, нейтрализовать и элиминировать. Существенное значение могут иметь нарушения соотношений между веществами антагонистами в гуморальных регуляторных системах (ферменты-антиферменты, оксиданты-антиоксиданты, цитокины-антицитокины и т.д.).
Исходя из взаимоотношений эндогенной интоксикации и возможностей функциональной системы детоксикации (ФСД) можно выделить 4 стадии развития эндотоксикоза: компенсации, напряжения, субкомпенсации и декомпенсации.
3. ПАТОГЕНЕЗ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
Механизм И в основном заключается в повреждающем действии эндогенного или экзогенного токсического агента на те или иные клеточные структуры и нарушении метаболических процессов в организме. При некоторых видах И повреждение клеток может иметь характер некроза (напр., при воздействии четыреххлористого углерода на печень), однако, в большинстве случаев происходят обратимые изменения на различных уровнях организма от субклеточного до системного, которые приводят к сдвигам гомеостаза в связи с нарушением метаболизма. Так, в основе мембранотоксического действия афлатоксинов, некоторых бактериальных токсинов, сапонинов лежит нарушение структуры фосфолипидов и образование промежуточных продуктов гидролиза. В механизмах И имеет значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс серотонина, кининов и других физиологически активных веществ, выделяющихся в значительных количествах при повреждении клеток и тканей.
В механизмах И имеют значение не только непосредственное действие токсических веществ на определенные функции, но и нейрогуморальные и рефлекторные влияния, а также вовлечение в патологический процесс различных органов и систем. При хронических И некоторыми химическими соединениями, алкилирующими фосфатные группы нуклеиновых кислот (нитрозоэтилмочевина, этилметан-сульфонат и др.), может проявиться их мутагенное действие; при И некоторыми циклическими углеводородами (3,4-бензпирен и др.) – канцерогенное действие.
Развитию И противостоят детоксицирующие системы организма, обеспечивающие химическое превращение токсичных веществ в менее токсичные или растворимые вещества, поддающиеся выведению из организма (окисление, гидролиз, метилирование, восстановление и образование парных соединений и другие процессы). Эти процессы происходят с участием ферментных систем организма, обеспечивающих обезвреживание и метаболические превращения ядовитых веществ. Яды, поступающие в кровь, через воротную вену попадают в печень, являющуюся мощным детоксицирующим барьером, и частично в ней нейтрализуются. И развивается при поступлении в организм токсичных веществ в количестве, превышающем возможности детоксицирующих систем или при их неполноценности.
4. КЛИНИКА ЭНДОГЕНОЙ ИНТОКСИКАЦИИ
По клиническому течению И делят на острые и хронические. Тяжесть И определяется величиной токсической дозы и реактивностью организма. Соответственно выделяют И легкой, средней и тяжелой степени.
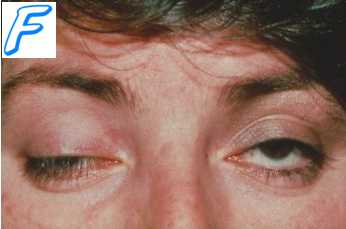
Клинические проявления эндогенных и экзогенных И имеют свои особенности. Течение эндогенной И в значительной степени определяется характером основного заболевания. Так, например, для диффузного токсического зоба характерны стойкая тахикардия, похудание, экзофтальм – симптомы токсического действия избыточного количества тиреоидных гормонов (тиреотоксикоз). При хронической уремии отмечаются явления воспаления в местах выделения азотистых шлаков; в гортани, глотке, желудочно-кишечном тракте, на коже обнаруживаются скопления кристаллов мочевины («уремическая пудра»). При хронической эндогенной И больные отмечают недомогание, раздражительность, разбитость, головную боль, головокружение, тошноту; наступает истощение, снижается резистентность организма. В ряде случаев эндогенная И может протекать в форме тяжелого острого отравления (рвота, ступор, коматозное состояние). Такое течение характерно для острой почечной недостаточности, гепатаргии, токсемического шока, острой ожоговой токсемии.
Течение экзогенной И определяется, в основном, токсикодинамикой яда, его дозой, способом попадания в организм, функциональным состоянием организма. Избирательность действия различных ядов обусловливает возникновение тех или иных синдромов: бронхоспазм, токсический отек легких, судороги. Тяжелая экзогенная И может протекать с нарушением дыхания и гемодинамики, преобладанием почечной и печеночной недостаточности, может наблюдаться коматозное состояние; при отравлении некоторыми ядами возможны интоксикационные психозы.
При длительном действии ядов в малых концентрациях (часто ниже минимально токсических доз) вначале возникают неспецифические симптомы в виде разнообразных нарушений функций преимущественно нервной и эндокринной систем, позднее присоединяются симптом специфических системных поражений (напр., марганцовый паркинсонизм, остеопороз при хроническом отравлении соединениями фтора и др.). Хроническая И некоторыми нейротропными ядами избирательного действия может с самого начала сопровождаться специфическими симптомами (миоз при отравлении мускарином, эзерином и подобными им веществами, сухость во рту и мидриаз при отравлении атропином). Иногда в процессе хронической И могут возникнуть бурно протекающие симптомы (например, свинцовая колика).
5. КЛИНИЧЕСКОЕ ОБСЛЕДОВАНИЕ ПАЦИЕНТОВ С СИНДРОМОМ ЭНДОГЕННОЙ ИНТОКСИКАЦИИ. УРОВНИ ДИАГНОСТИКИ
Диагностика ЭИ разработана главным образом на биохимическом уровне.
В том случае, если состояние не является критическим, для его диагностики целесообразно использовать тот же принцип, что и заложенный в основу распознавания дистресса, т.к., по-видимому, эндогенная интоксикация во многом пересекается с реакцией общего адаптационного синдрома. Мы предлагаем оценивать такие признаки дистресса, главным образом субъективные, которые составляют основу ряда вопросников для диагностики дистресса (табл. 1).
Шкала для диагностики хронической эндогенной интоксикации.
Что такое острый эндотоксикоз
ПОНЯТИЕ И КЛАССИФИКАЦИЯ ЭНДОТОКСИКОЗА,
ЭНДОГЕННОЙ ИНТОКСИКАЦИИ
И ЭНДОГЕННЫХ ТОКСИЧЕСКИХ СУБСТАНЦИЙ
Эндотоксикоз представляет собой типовой патологический процесс, являющийся структурно-функциональным ответом организма на токсическую агрессию как эндогенной, так и экзогенной природы. С более узкой практической точки зрения его можно охарактеризовать как клиническое проявление эндогенной интоксикации, которая не сдерживается механизмами адаптации и компенсации токсической информации.
При остром эндотоксикозе эндогенная интоксикация неуклонно прогрессирует несмотря на развитие и напряжение компенсаторных механизмов (содержание и диапазон ЭТС прогрессивно увеличиваются), что приводит к нарушению регуляции гомеостаза, к формированию синдрома множественной органной несостоятельности, дезинтеграции функций организма и нередко к летальному исходу.
Подострый (затяжной) эндотоксикоз можно рассматривать как вариант острого эндотоксикоза, который характерен для медленно (в течение нескольких дней или даже недель) прогрессирующего патологического состояния. Компенсаторные реакции длительное время сдерживают его прогрессирование. В дальнейшем, при отсутствии эффективного лечения, происходит срыв компенсаторных механизмов и быстрое развитие плохо корригируемых метаболических нарушений, как правило, приводящих к летальному исходу.
В развитии острого эндотоксикоза одновременно или последовательно могут участвовать несколько механизмов образования ЭТС и накопления их во внутренней среде организма.
Острый эндотоксикоз протекает как каскадный процесс. Развитие и прогрессирование его связано с несоответствием между образованием (поступлением и т.д.) токсических субстанций, в том числе образующихся в результате последующей токсической аутоагрессии, и способностью органов, входящих в функциональную систему детоксикации (легкие, печень, почки, ЖКТ, кожа, система иммунологического надзора), их трансформировать, нейтрализовывать и элиминировать. Существенное значение могут иметь нарушения соотношений между веществами антагонистами в гуморальных регуляторных системах (ферменты-антиферменты, оксиданты-антиоксиданты, цитокины-антицитокины и т. д.) [29].
Исходя из взаимоотношений эндогенной интоксикации и возможностей функциональной системы детоксикации (ФСД) можно выделить 4 стадии развития эндотоксикоза (табл. 16.1 [показать] ).
| Таблица 16.1. Стадийность острого эндотоксикоза | ||||||||||||||||
| Стадия эндотоксикоза | Эндогенная интоксикация | Функциональная система детоксикации (ФСД) | ||||||||||||||
| 1) компенсации | Появление избытка первичных ЭТС | Адекватное усиление работы ФСД | ||||||||||||||
| 2) напряжения | Развитие вторичной аутоагрессии | Неадекватное усиление работы ФСД | ||||||||||||||
| Дисфункция органов ФСД | ||||||||||||||||
| 3) субкомпенсации | Прогрессирование вторичной аутоагрессии | Недостаточность ФСД и органов жизнеобеспечения | ||||||||||||||
| 4) декоменсация | Развитие жизнеугрожающих нарушений | Несостоятельность ФСД и органов жизнеобеспечения | ||||||||||||||
В стадии компенсации ФСД полностью компенсирует токсемическую нагрузку. В стадии напряжения скорость наработки токсических субстанций совпадaет с максимальными возможностями ФСД. В стадии субкомпенсации наработка токсических субстанций определенно превышает возможности ФСД. И наконец в стадии декомпенсации развивается несостоятельность органов ФСД и появляются жизнеугрожаюшие метаболические и функциональные нарушения.
Концентрация любой ЭТС в конкретной клинической ситуации отражает результирующую скоростей образования этой субстанции, скоростей ее накопления и распределения в тканевых и клеточно-мембранных депо и скорости его биотрансформации или элиминации основными и дополнительными путями (рис. 16.1).
Все эти подходы могут найти реализацию в практической деятельности лабораторной службы, обеспечивающей ежедневную деятельность блоков и отделений реанимации и интенсивной терапии, кабинетов, отделений и центров экстракорпоральной гемокоррекции.
| Таблица 16.2. Алгоритм диагностики острого эндотоксикоза | |
| Показатели | Цель исследования |
| Показатели, характеризующие начальную токсинемию | Установить наличие значительной интоксикации и, возможно, получить информацию о ее источнике |
| Маркеры вторичной токсической аутоагрессми: Группа маркеров интоксикации и показателей интегральной токсичности биологических жидкостей (кровь, лимфа, моча, слюна, ликвор) | Интегрально оценить степень выраженности эндогенной интоксикации |
| Показатели, характеризующие баланс гуморальных регуляторных систем | Выявить нарушения соотношений между веществами антагонистами |
| Показатели, характеризующие функционирование органов и систем, в первую очередь функциональной системы детоксикации | Определить, какие жизненно важные органы поражены и каковы функциональные резервы остальных |
| Базисные (организменные) клинико-функциональные и лабораторные показатели | Показать, угрожает ли первичная токссинемия и эндотоксикоз существованию организма и в чем это выражается |
ДИАГНОСТИКА НАЧАЛЬНОЙ ТОКСИНЕМИИ
Определение уровня лактата крови на фоне критического состояния организма больного и гипергликемии позволяет оценить выраженность лактоацидоза, но только его сопоставление с другими показателями углеводного обмена позволяет отнести это явление к постгипоксическому ацидозу или к лактоацидозу как проявлению критической декомпенсации сахарного диабета. Другим вариантом, подтверждающим наличие диабетогeнной природы эндогенной интоксикации, считается определение кетоновых тел, особенно если оно соотносится с данными исследования кислотно-основного состояния крови и уровнем осмолярности.
При оценке глубины ЭнИ при механической желтухе можно ориентироваться на уровень билирубина крови, который соотносится с выраженностью психических расстройств и тяжестью гепатоцеллюлярной несостоятельности. Однако во многих случаях информации только об уровне и динамике гипербилирубинемии явно недостаточно для диагностики эндотоксикоза на фоне печеночной несостоятельности.
Устойчивое повышение плазменного уровня калия (гиперкалиемия выше 6 ммоль/л) позволяет думать об опасности дальнейшей его задержки в организме с развитием критического состояния и жизненной необходимости активной детоксикации. Это должно особенно привлечь внимание, если существенно снижено мочеотделение и определяются признаки гиперкалиемии на ЭКГ.
Высокий уровень азотистых шлаков в крови (остаточного азота, мочевины, мочевой кислоты) позволяет связывать развитие начальной токсинемии с поражением почек и ретенцией этих токсических субстанций, хотя возможен и продукционный механизм развития азотемии. Обычно на фоне многих вариантов ЭнИ имеется сочетание этих двух механизмов. Приходится расширять исследование, чтобы оценить преимущественный характер этого нарушения: наряду с мочевиной исследовать остаточный азот крови, а также определять индекс расщепления, то есть долю полипептпдов в общем пуле остаточного азота. В норме индекс расщепления равен 0,16-0,24; при продукционной азотемии он возрастает более 0,32. Возможен и чисто ретенционный характер азотемии, который связан с электролитными расстройствами в форме хлорипривной азотемии. Она обычно наблюдается при гипохлоремическом гипокалиемическом алкалозе, что дополнительно требует определения концентрации ионов хлора и бикарбоната в плазме крови и во внеклеточной жидкости.
Определение активности панкреатических ферментов в сыворотке крови, особенно протеиназ и липаз и их ингибиторов, может характеризовать уровень энзимно-продукционной ЭнИ при деструктивном панкреатите. Определенное значение при этом имеет локус забора крови на исследование. Если представлять значение легких как органа детоксикации, наибольшую информацию о маркерах данного вида ЭнИ может предоставить смешанная венозная кровь (из центральной вены или правого предсердия), дающая представление об уровне данных маркеров до того, как такая токсическая информация будет «переработана» легкими.
Намного точнее глубину патологического процесса в поджелудочной железе отражает исследование панкреатических ферментов в лимфе грудного лимфатического протока (если он дренирован с целью детоксикации).
Этот подход выявляет значение лимфатической системы в транспорте ЭТС из интерстиция поврежденных органов в кровь. Определенную информацию может предоставить исследование белкового спектра лимфы и ее коллоидно-осмотического давления (КОД). У больных с выраженной интоксикацией анализ первых ее проб выявляет тенденцию к повышению оощего белка (выше 40 г/л) с увеличением концентрации грубодисперсных белков (IgМ, сиалопротеины, гаптоглобины и другие макроглобулины), что свидетельствует о наличии не только диспротеинемии, но и деструктивно-дегенеративного процесса, вызывающего интоксикацию.
На начальной стадии септицемии определение микробных липополисахаридов с помощью ЛАЛ-теста, в котором основным реагентом выступает лизат амебоцитов сухопутного краба Limulus Poliphemus, позволяет достаточно объективно судить об уровне микробного фактора эндогенной интоксикации. Но этот же тест может указывать на значительный уровень эндотоксинемии н в отсутствие четко определяемого очага гнойной инфекции, например, при так называемом «септическом синдроме», который выявляется на фоне рефрактерного циркуляторного шока.
Несомненно, представляет интерес изучение содержания регуляторных факторов (гормонов, биологически активных веществ и медиаторов тканевого обмена и медиаторов воспаления) в качестве ЭТС. Действительно, выявление патологического уровня тиреоидного гормона или регуляторного пептида, например, вазоинтестинального пептида, или простагландинов позволяет судить о выраженности ЭнИ и предполагать пути ее дальнейшего развития. Важную информацию для определения тактики лечения может предоставить и исследование первичных мессенджеров иммунного ответа ИЛ-1 и ФНО. Но эти методики доступны только крупным отечественным стационарам и диагностическим центрам.
Среди тестов, отражающих иммунопатологические влияния первичного аффекта эндотоксикоза, наиболее часто используют исследования тканевых антигенов, уровня цикулирующих иммунных комплексов (ЦИК) и комплемента крови. Во всяком случае, повышение концентрации ЦИК при одновременном снижении уровня С3-компонента комплемента может свидетельствовать об избыточности образования иммунных комплексов. Они могут стать как фактором первичного патогенного воздействия, так и фактором вторичной аутоагрессии и способствовать тканевым и органным проявлениям эндотоксикоза.
| Страница 1 2 3 | всего страниц: 3 |
Источник: Медицинская лабораторная диагностика, программы и алгоритмы. Под ред. проф. Карпищенко А.И., СПб, Интермедика, 2001