Что такое печеночная гастропатия
Гастропатия: причины, виды, симптомы
Пациенты часто путают гастрит и гастропатию, между тем – это совершенно разные понятия. Если при гастрите определяются явные признаки воспалённого состояния слизистой оболочки желудка, то гастропатия – группа различных заболеваний желудка, характеризующихся повреждениями его эпителия, сосудистой системы. Воспаления при гастропатии также возможны, но они носят совершенно незначительный характер.
Каждый второй житель планеты страдает нарушениями органов пищеварения, а в возрасте старше 50 лет их больше 60%. Из-за гормональных проблем гастропатия среди женщин диагностируется немного чаще чем среди мужчин. По распространенности же у детей гастропатия занимает второе место после респираторных инфекций.
Причинами возникновения гастропатии могут быть как внешние так и внутренние причины. Наиболее частые из них:
Среди факторов риска:
Отметим также, что любое игнорирование проблем со здоровьем чреваты серьёзными рисками для развития гастропатий.
На начальных стадиях гастропатии симптомы, как правило, отсутствуют. Первые признаки могут скрыть симптомы, характерные для других заболеваний и патологий – это обстоятельство способствует развитию заболевания. В дальнейшем же гастропатия проявит себя тяжестью в желудке, изжогой, отрыжкой, тошнотой, иногда рвотой, метеоризмом.
В грудном и детском возрасте гастропатия чаще всего проявляет себя в острой форме и характеризуется внезапным появлением и быстрым течением. «Спусковым крючком» для развития заболевания может стать переход на искусственное вскармливание, воздействие пищевых аллергенов, лекарственные препараты, испорченные продукты и молочные смеси. Заболевание проявляется общим недомоганием, беспокойством, болями в области желудка и пупка, отсутствием аппетита, тошнотой, рвотой, поносом. Острая стадия может перейти в хроническую, для которой характерны «голодные» боли, чувство распирания и переполнения желудка. Хроническая стадия может стать сопровождать ребёнка продолжительный отрезок его жизни.
В зависимости от того, насколько повреждены эпителиальные клетки внутренней поверхности желудка, от того как негативные факторы повлияли на ткани желудка, различают следующие виды заболевания, из которых чаще всего встречаются:
Помимо перечисленных существует еще более десятка вида гастропатий: атрофическая, антральная, катаральная, гиперпластическая, гипертрофическая, диффузная, рефлюкс-гастропатия, портальная, ассоциированная, экссудативная (болезнь Менетрие), зернистая, лимфоидная, рекативная, язвенная, уремическая, индуцированная.
Встречается и смешанная гастропатия, возникающая в результате развития сразу нескольких ее форм.
При диагностике гастропатий, медики используют несколько классификаций заболевания. Как уже упоминалось ранее, гастропатия может иметь острую и хроническую формы. По степени развития гастропатию классифицируют по степеням, где:
Стадии заболевания определяются характером протекания, длительностью болезни, эффективностью лечения, состоянием внутренней поверхности желудка:
Несвоевременно выявленая гастропатий, позднее начало ее леченияможет вызвать целую группу осложнений, выражающихся в нарушении пищеварения из-за недостаточной выработки желудочного сока и пепсина, застойных явлений в антральном отделе желудка. Последствиями может стать развитие В12-дефицитной анемии вследствие нарушения всасывания желудком полезных веществ, образование опухолей, вплоть до злокачественных, желудочное кровотечение.
Диагностика гастропатии проводится гастроэнтерологом.
При подозрении на гастропатию проводят гистологический анализ путём исследование взятого образца ткани (биоптата). Для этого с участков видимых повреждений и здоровых, соседствующих с ними, отдельно берётся материал. Такой анализ позволяет определить некоторые виды хронического гастрита или установить характер новообразований. Для определения состояния слизистой применяются два вида теста: на кислотность (внутрижелудочная РН-метрия) и на соотношение пепсиногена I и пепсиногена II в плазме – проферментов, вырабатываемых фундальными железами желудка. Также проводится анализ на наличие бактерии хеликобактер пилори, возможно и биохимическое генетическое исследование. Стандартной является процедура проведение общего и биохимического анализа крови, анализ мочи (для определение уровня уропепсина) и кала (копрограмма).
При диагностике гастроскопии также выполняют УЗИ органов брюшной полости.
Напоминаем: поставить точный диагноз, назначить лечение может только квалифицированный специалист!
Записаться на прием к гастроэнтерологу в Профессорскую клинику (ул Дружбы, 15а) можно по единому телефону в Перми 206-07-67, или воспользовавшись сервисом «Запись на прием» на нашем сайте. При необходимости, специалист назначит необходимые лабораторные и инструментальные диагностические процедуры, большинство из которых можно также выполнить в Профессорской клинике
Что такое печеночная гастропатия
У больных циррозом печени (ЦП) вирусной этиологии частота развития портальной гастропатии (ПГ) составляет около 50–70 % [9]. Клинически ПГ протекает чаще бессимптомно, но может проявлять себя как острое или хроническое желудочное кровотечение с признаками железодефицитной анемии (ЖДА). Геморрагические проявления на слизистой оболочке желудка и формирование анемии у больных хроническими вирусными заболеваниями печени являются неблагоприятными прогностическими признаками, существенно влияющими на качество жизни пациентов. С учетом вышеизложенного ранняя диагностика и своевременная профилактика ПГ в сочетании с правильной этиотропной и патогенетической терапией может существенно улучшить прогноз заболевания у больных хроническим вирусным гепатитом (ХВГ).
Этиология и патогенез
Патогенез синдрома ПГ на сегодняшний день остается малоизученным. Предполагается, что ведущую роль в развитии ПГ играет повышение давления в портальной системе с шунтированием крови в портокавальных анастомозах. В нормальных условиях давление крови в системе воротной вены составляет 4–6 мм рт. ст., при ЦП оно может подниматься до 25–30 мм рт. ст. с развитием коллатеральной циркуляции, при этом портальная гипертензия поддерживается за счет гипердинамического типа кровообращения. Отмечена прямая зависимость между тяжестью ПГ, величиной портопеченочного давления, индексом портального полнокровия и степенью дисфункции печени (согласно критериям Child–Pugh) [1, 4]. Увеличение притока венозной крови к слизистой оболочке желудка вызывает расширение ее капилляров, способствует застойным явлениям и гипоксии [1, 7]. Это приводит к гипертрофии эндотелия сосудов и делает его более чувствительным к повреждающим агентам [14]. Кроме того, данные изменения гемодинамики способствуют увеличению выработки фактора некроза опухоли α и простагландинов, которые активируют содержащуюся в слизистой оболочке желудка эндотелиальную NO-синтазу и эндотелин-1 [7, 15]. Повышенная продукция NO, эндотелина-1, а также сосудистого эндотелиального фактора роста индуцирует образование тромбов, разрыв венул и внутрислизистые кровоизлияния. Развившаяся гипоксия тканей и усиление перекисного окисления липидов определяют ишемический компонент в повреждении железистых клеток, что усугубляет проявления ПГ [1, 2].
В развитии ПГ существенное значение может играть повышенное содержание гастрина в крови при снижении инактивации его в печени из-за печеночно-клеточной недостаточности, что может приводить к снижению секреции гидрокарбонатов и расстройствам желудочного слизеобразования. Уменьшение продукции слизи происходит в результате нарушения функции мукоцитов и является дополнительным фактором, снижающим резистентность слизистой оболочки желудка [1, 6].
Вероятность развития кровотечения из слизистой оболочки желудка при ПГ возрастает при полипрогмазии (одновременном применении более 4 лекарственных препаратов), применении нестероидных противовоспалительных средств, лечении гепатопротекторами [3].
На стадии изучения находится вопрос о связи ПГ с Helicobacter рylori. Имеются работы, доказывающие отрицательное влияние Н. рylori на ПГ. При этом ряд исследователей не находят связи между степенью колонизации Н. рylori и тяжестью ПГ [6].
Склерозирование варикозно расширенных вен пищевода значительно усиливает сосудистую эктазию слизистой оболочки желудка при ПГ, что может способствовать кровотечению [1, 3, 11].
Факторы, способствующие развитию ПГ:
• повышение давления в портальной системе;
• повышенная продукция NO, эндотелина-1, сосудистого эндотелиального фактора роста;
• повреждение железистых клеток желудка и уменьшение продукции слизи;
• повышенное содержание гастрина в крови при снижении инактивации его в печени из-за печеночно-клеточной недостаточности;
• полипрогмазия, лечение гепатопротекторами, НПВС;
• возможно, течение ПГ усугубляется наличием Н. рylori;
• лигирование и склерозирование вен пищевода.
Морфологически ПГ проявляется увеличением количества артериовенозных шунтов между подслизистым слоем и слизистой оболочкой желудка, расширением прекапилляров и венул подслизистого слоя, т. е. сосудистой эктазией. При ПГ биопсия слизистой оболочки из кардиального отдела желудка позволяет обнаруживать расширение прекапилляров, фиброзно-мышечную гиперплазию и периваскулярный фиброз [1, 3, 6, 7].
Клинические проявления
ПГ может протекать в различных клинических вариантах, чаще всего бессимптомно или с минимальными проявлениями (жалобы на дискомфорт в эпигастрии, изжогу, отрыжку, незначительную слабость). В отсутствие патогенетического лечения ПГ прогрессирует до развития кровотечения непосредственно из слизистой оболочки желудка и проявляется клинически гипохромной ЖДА, которая при ЦП усугубляется нарушением свертываемости [1, 3]. Патология системы крови – частое осложнение ХВГ и наблюдается более чем у половины больных [3].
Об остром кровотечении у больных ПГ свидетельствуют жалобы на рвоту с кровью (кофейной гущей) или черный стул (мелену) при обязательном лабораторном подтверждении (снижении содержания гемоглобина в периферической крови, железа – в сыворотке крови). Окончательный диагноз устанавливается после исключения кровотечения из варикозно расширенных вен пищевода или других источников кровопотери. Хроническое кровотечение, ассоциированное с ПГ, чаще всего выявляют при плановом обследовании по поводу ЖДА. После чего больной направляется к гастроэнтерологу, от квалификации которого зависит правильная интерпретация патологии желудка. Часто проходят годы до установления диагноза ХВГ и, соответственно, начала правильного этиотропного и патогенетического лечения [2, 3, 5]. Однако в большинстве случаев диагноз ПГ и как следствие – гипохромная ЖДА ставятся уже на фоне известного ХВГ [6, 15].
Ведение больных ХВГ предусматривает лечение основного заболевания и профилактику осложнений, в т. ч. ПГ и ЖДА, для чего обязательно соблюдение стандартов обследования. Всем пациентам с впервые диагностированным ЦП или подозрением на него необходимо выполнять эзофагогастродуоденоскопию (ЭГДС) с целью выявления ПГ. Дальнейшая частота ЭГДС зависит от эндоскопической картины и степени поражения печени по критериям Child–Pugh [1] (табл. 1).
Оптимальные результаты профилактики и лечения ПГ достигаются на стадии ЦП, соответствующей классу А.
Ключевым методом в диагностике ПГ является эндоскопическое исследование желудка. На согласительной конференции по вопросам эндоскопии желудка при портальной гипертензии (Милан, Италия, 19 сентября 1992 г.) ПГ определена как изменение слизистой оболочки желудка в виде небольших полигональных участков розового цвета, слегка выступающих к центру по типу “мозаики”.
Определены три основных эндоскопических признака:
1 – мелкие красные точки на слизистой оболочке желудка диаметром менее 1 мм;
2 – красные пятна диаметром более 2 мм;
3 – черно-коричневые пятна, являющиеся следствием внутрислизистых геморрагий [6, 9, 14].
K. Tanoue и соавт. классифицировали ПГ по трем степеням тяжести:
• 1-я ст. – небольшая гиперемия отдельных участков слизистой оболочки желудка, слизистая оболочка имеет “застойный” вид.
• 2-я ст. – выраженное покраснение с участками возвышающейся отечной слизистой оболочки желудка, разделенными тонкой белой сетью, – изменения по типу “мозаики”.
• 3-я ст. – точечные геморрагии на фоне макроскопических изменений, характерных для 2-й ст. [7].
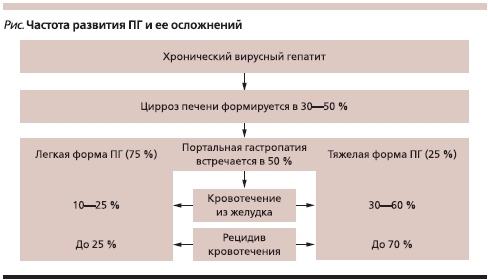
Наиболее простая классификация (T.T. McCormack и соавт.) предполагает две степени поражения слизистой оболочки желудка. При ПГ легкой степени эндоскопически выявляют мозаичный рисунок слизистой оболочки, при тяжелой – в дополнение к мозаичному рисунку появляются диффузные темно-красные пятна, подслизистые геморрагии. Эта классификация удобна для прогнозирования вероятности развития кровотечения. Так, при легкой степени ПГ, которая выявляется в 75 % случаев у всех больных ПГ, риск кровотечения составляет до 25 %. При тяжелой степени ПГ, встречающейся в 25 % случаев, частота кровотечений увеличивается до 60 %, которые могут оказаться фатальными (см. рисунок) [9].
Лечение и профилактика
При наличии клинических признаков ПГ при ХВГ рекомендуется применение комбинированного лечения противовирусными препаратами и средствами, направленными на нормализацию состояния слизистой оболочки желудка и предотвращение кровотечений (табл. 2).
Для профилактики осложнений ПГ наиболее оправданным остается применение неселективных β-адреноблокаторов, эффективных при лечении пациентов с гипердинамическими нарушениями кровообращения, наблюдающимися при ЦП, и способствующих снижению давления в воротной вене, уменьшая риск кровотечения [1, 10, 11]. С этой целью используют пропранолол, который назначают в дозе от 10 до 120 мг 2 раза в сутки [13].
Важным направлением терапии ПГ является применение ингибиторов протонового насоса желудка, оказывающих антисекреторное действие, ингибируя АТФазу париетальных клеток слизистой оболочки желудка, что приводит к уменьшению секреции соляной кислоты. Представители этой группы – омепразол, эзомепразол, пантопразол. Пантопразол назначают внутрь 40–80 мг/сут в 2 приема. Для защиты слизистой оболочки желудка применяются Н2-блокаторы – ранитидин, фамотидин, участвующие в регуляции секреторной деятельности желудка. Ранитидин назначают по 0,3 г 1 раз вечером в течение 4–8 недель [1, 4, 5, 10].
При ПГ оправданно применение обволакивающих средств, обладающих и антацидными свойствами, – Альмагель (по 1 дозированной ложке 3 раза в сутки за 30 минут до еды и перед сном); алюминия фосфат (по 1–2 пакетика 50 %-ного геля 2–3 раза в сутки); висмута трикалия дицитрат (0,12 г 4 раза в сутки за 30 минут до еды и перед сном, спустя 2 часа после еды, курс лечения – 6–8 недель) [4, 5].
Если у пациентов с ПГ выявляется Н. рylori, необходимо проведение антибактериальной терапии [6, 10]. При острых кровотечениях наибольшую эффективность за счет снижения полнокровия слизистой оболочки желудка показал октреотид – синтетический аналог гормона соматостатина, способный редуцировать портальное давление с умеренным уменьшением печеночной перфузии [12]. Для лечения гипохромной ЖДА применяют препараты железа (железа (III)-гидроксид полиизомальтоза для внутримышечных введений), для коррекции выраженной анемии используются внутривенные формы железа (железа (III)-гидроксид декстрана комплекс, железа (III)-гидроксид сахарозный комплекс) [3, 15]. Консервативная эндоскопическая терапия кровотечений при ПГ применяется редко и заключается в использовании эндоскопической (аргоноплазменной) коагуляции [8, 10].
Результаты собственных наблюдений
Мы проанализировали 507 историй болезни пациентов с хроническим гепатитом С (ХГС) и ХГВ, наблюдавшихся в стационарах и поликлиниках общетерапевтического профиля Москвы. ХГС был диагностирован 323 (63,2 %) больным, ХГВ – 184 (36,8 %). Среди обследованных пациентов было 216 (42,3 %) женщин и 295 (57,7 %) мужчин.
Диагноз ПГ обследованным пациентам ставился в период от первичного обращения к терапевту до начала проведения противовирусной терапии. Все пациенты, включенные в исследование, прошли необходимые обследования, включившие серологическое исследование, ПЦР (полимеразную цепную реакцию)-диагностику, общий анализ крови и мочи, биохимическое исследование крови, ультразвуковое исследование брюшной полости, ЭГДС, в отдельных случаях компьютерную томографию, пункционную биопсию печени, ФиброМакс и эластографию.
В нашем исследовании клинические проявления ЦП имели место у 150 (29,6 %) больных, в т. ч. у 90 (17,8 %) больных – ХГС, у 60 (11,8 %) – ХГВ. Среди них признаки ПГ выявлены у 59 (36,8 %) пациентов, из них 33 (22 %) больны ХГС, 26 (17,3 %) – ХГВ.
ЖДА (снижение среднего объема эритроцитов, низкий уровень сывороточного железа и повышение общей железосвязывающей способности сыворотки) как следствие кровотечения при ПГ имела место в 22 (37,3 %) случаях, включая 12 (20,4 %) пациентов с ХГС, 10 (16,9 %) – с ХГВ.
Кровотечения легкой степени зарегистрированы у 32 (54,3 %) человек, которым проведена терапия в соответствии с установленными стандартами. Повторные кровотечения развились при тяжелой степени ПГ в 11 % случаев.
Таким образом, ПГ – это распространенное осложнение хронических вирусных заболеваний печени на стадии формирования ЦП, которое часто сопровождается кровотечением и ЖДА. Многие звенья этиологии и патогенеза ПГ на сегодняшний день до конца не изучены и нуждаются в углубленном исследовании. Правильное и своевременное соблюдение утвержденных стандартов обследования и лечения позволит сократить риск развития ПГ. В лечении ПГ, проводимом на фоне противовирусной терапии, оправданным остается применение β-адреноблокаторов, антацидов, блокаторов протонной помпы; лечение наиболее эффективно на ранних стадиях ЦП.
Литература
1. Шерлок Ш., Дули Дж. Заболевания печени (пер. с англ.) / Под ред. З.Г. Апросиной, И.А. Мухина. М., 1999. 864 с.
2. Абдурахманов Д.Т. Хронический гепатит B и D. М., 2010. 267 с.
3. Практическая гепатология / Под редакцией Н.А. Мухина. М., 2004. 294 с.¬
4. Майер К.П. Гепатит и последствия гепатита. М., 2004. 717 с.
5. Рекомендации по лечению гепатита С (Согласительная конференция по лечению гепатита С, Франция, 27–28 фев. 2002 г.) // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии 2003. № 2. С. 4–12.
6. Гарбузенко Д.В. Гастропатия, ассоциированная с портальной гипертензией // РМЖ 2004. № 4. С. 44–5.
7. Хомерики С.Г., Мельникова С.В., Обуховский В.И., Яковенко Э.П. Клинико-морфологические проявления гастропатии у больных портальной гипертензией // Гепатология 2005. № 1. С. 8–15.
8. Bhasin DK, Malhi NJ. Variceal bleeding and portal hypertension: much to learn, much to explore Endoscopy 2002;34:119–28.
9. Pique JM. Portal hypertension gastropathy Baillieres Clin. Gastroenterology 1997;11: 257–70.
10. Seewald S, Seitz U, Yang AM, Soehendra N. Variceal bleeding and portal hypertension: still a therapeutic challenge? Endoscopy2001;33:126–39.
11. Comar KM, Sanyal AJ. Portal hypertensive bleeding. Gastroenterol Clin N Am 2003;32: 1079–105.
12. Escorsell A, Bandi JC, Andreu V, et al. Desensitization to the effects of intravenous octreotide in cirrhotic patients with portal hypertension. Gastroenterology 2001;120: 161–69.
13. Perez-Ayuso RM, Pique JM, Bosch J, et al. Propranolol in prevention of recurrent bleeding from severe portal hypertensive gastropathy in cirrhosis. Lancet 1991;337:1431–34.
14. Primignani M, Carpinelli L, Preatoni P, et al. Natural history of portal hypertensive gastropathy in patients with liver cirrhosis. The New Italian Endoscopic Club for the study and treatment of esophageal varices (NIEC). Gastroenterology2000;119:181–87.
15. Sarin SK, Shahi HM, Jain M, et al. The natural history of portal hypertensive gastropathy: influence of variceal eradication. Am J Gastroenterol2003;98:1758–65.
Что такое печеночная гастропатия
Для продолжения изучения на мобильном устройстве ПРОСКАНИРУЙТЕ QR-код с помощью спец. программы или фотокамеры мобильного устройства
Случайный выбор
данная функция, случайным образом выбирает информацию для Вашего изучения,
запустите выбор нажав кнопку ниже
Случайный выбор
Обратная связь
Напишите нам
Сообщение об ошибке
Что улучшить?
Введение:
Полный текст статьи:
Эндоскопическая картина
Картина слизистой (ее еще иногда описывают как «кожу аллигатора» или «змеиную кожу») представляет собой множественные небольшие полигональные приподнятые участки красной (розовой или вишневой) слизистой разделенные ретикулярной сетью прожилок белесого или желтоватого цвета. В более тяжелых случаях такая картина дополняется подслизистыми кровоизлияниями и даже просачиванием крови из слизистой желудка. Данная патология наиболее часто локализуется в теле и дне желудка [14]. ПГГ часто, но далеко не обязательно, сочетается c варикозно расширенными венами пищевода или желудка.
При морфологическом исследовании выявляются расширенные вены и капилляры слизистой и подслизистого слоя без воспалительных и эрозивных изменений [4].
Классификация
Течение
Вопросы патогенеза данного состояния продолжают быть предметом дискуссий, считается, что в его основе лежит портальная гипертензия. Ohta M. Et al. [6] описывает возможный механизм развития ПГГ следующим образом: увеличенное портальное давление запускает изменения местной гемодинамики вызывая застойные изменения в дне и теле желудка и повреждение его слизистой, что в свою очередь вызывает активацию цитокинов и фактора роста, что активирует синтез оксида азота и эндотелин 1. Оксид азота вызывает гипердинамическую циркуляцию и гиперпродукцию пероксинитрита. Он в сочетании с эндотелином 1 повышает чувствительность слизистой желудка к повреждению. Как уже было сказано выше ПГГ одинаково часто развивается у пациентов с портальной гипертензией ассоциированной с поражением печени и другими причинами [1]. Точной зависимости между тяжестью гипертензии и вероятностью ПГГ не выявлено [2]. Более того, ПГГ имеет достаточно непредсказуемое течение, возникая, меняя степени тяжести и даже спонтанно проходя [9].
Лечение
Эндоскопическая терапия малоэффективна т.к. кровотечение чаще всего носит невыраженный и диффузный характер. При визуализации конкретной токи кровотечения можно использовать инъекционную терапию или коагуляцию термическим зондом или лазером. Хотя исследований посвященных эффективности/безопасности данного подхода нами в доступной литературе не найдено.
Соматостатин и октреотид снижаю кровоток в слизистой желудка, однако этот эффект носит транзисторный характер. Например, время действия октреотида оценивалось в 5 минут, причем его продленная инфузия снижения портального давления не давало, а повторное введение имело менее выраженный эффект [3]. Применение соматостатина у больных с ПГГ ассоциированным кровотечением (26 человек) в дозе 250 мкг болюсно приводило к остановки кровотечения у всех пациентов [4]. Рекомендуется применять соматостатин (октреотид) для остановки острого кровотечения, а b-блокаторы для профилактики его рецидива и контроля хронического кровотечения.
Что такое печеночная гастропатия
Шерцингер А. Г., Жигалова С. Б., Семенова Т. С., Цаава Д. В.
Федеральное государственное бюджетное учреждение «Российский научный центр хирургии имени академика Б. В. Петровского» Российской академии медицинских наук
г. Москва
Портальная гипертензионная гастропатия (ПГГ) – совокупность вторичных макроскопических и микроскопических изменений слизистой и подслизистой оболочек желудка, заключающаяся в расширении сосудов этих слоев в результате венозного стаза, возникающих при портальной гипертензии любого генеза.
Распространенность ПГГ колеблется от 9,1 до 80%. Подобное расхождение может быть связано с несколькими факторами: отсутствием единых диагностических критериев и классификации, а также с различием в интерпретации поражений при эндоскопическом осмотре. Среди больных циррозом печени ПГГ встречается в 20 — 98% наблюдений. При этом в 65—90% случаев — ПГГ легкой, умеренной степени тяжести, а в 10—25% случаев — тяжелой степени.
ПГГ является потенциальным источником острого или хронического желудочного кровотечения. Смертность от острых кровотечений, связанных с ПГГ, составляет около 12,5%. Хронические кровопотери приводят к выраженным нарушениям функции печени, возникновению и прогрессированию печеночной энцефалопатии, значительно утяжеляя состояние больного.
Портальная гипертензионная гастропатия не имеет патогномоничных клинических симптомов. Заподозрить наличие патологии можно при выявлении стойкой, не корригируемой анемии у пациентов с ПГ, что может свидетельствовать о хронической кровопотере. Однако ориентироваться на изменение концентрации гемоглобина не стоит, так как данный показатель не является специфичным для больных с хроническими заболеваниями печени. Так же ПГГ может осложниться острым кровотечением в 2-12% случаев, но не является самой частой его причиной.
Золотым стандартом диагностики ПГГ является эзофагогастродуоденоскопия. Методика позволяет выявить характерные изменения слизистой оболочки проксимальных отделов желудка, их локализацию и распространенность, уточнить степень гастропатии, а при кровотечении — исключить варикозно расширенные вены пищевода и желудка как возможный источник геморрагии.
Морфологические проявления ПГГ до сих пор четко не определены. При гистологическом исследовании слизистой оболочки желудка выявлены признаки, характеризующие состояние слизистой оболочки желудка при портальной гипертензии – хронический венозный застой и гипердинамическая циркуляция, приводящие к повышенному кровенаполнению в слизистой оболочке, расширение капилляров и увеличение числа подслизистых артериовенозных сообщений, с растянутыми артериолами, капиллярами и венами в стенке желудка без воспалительного компонента в виде мононуклеарной клеточной инфильтрации. Исследования ультраструктуры выявляют экстравазацию эритроцитов в межэпителиальное пространство у больных с гастропатией.
Зачастую в литературе можно встретить ассоциативное восприятие «красных пятен» гастропатии и «красных стигматов» на слизистой оболочке пищевода, известных как васкулопатия. Однако имеются четкие морфологические различия между этими патологическими состояниями, несмотря на единый патогенетический механизм их развития. Вишнево-красные пятна васкулопатии представляют собой расширенные интраэпителиальные вены в слизистой оболочке пищевода, связанные с поверхностным и далее с глубоким венозными сплетениями. Красные пятна гастропатии представляют собой экстравазацию эритроцитов на уровне микроциркуляторного русла. Возникает закономерный вопрос: является ли наличие красных пятен гастропатии таким же стигматом угрозы кровотечения из варикозных вен желудка как наличие васкулопатии при ВРВ пищевода? Нам представляется, что нет. Гастропатия, несомненно, может сама стать источником геморрагии, но исследований, определяющих прогноз кровотеченией из варикозных вен желудка при наличии ПГГ, нами не найдено.
Большое количество существующих классификаций ПГГ свидетельствует о нерешенности данного вопроса. В своей работе мы используем следующую трех степенную классификацию ПГГ:
Основной причиной развития ПГГ по мнению большинства авторов остается портальная гипертензия. При изучении патогенеза гипертензионной портальной гастропатии предложены самые различные механизмы, в той или иной степени вовлеченные в формирование данного патологического состояния.
Повышение портального давления может вызвать изменения местной гемодинамики, в результате чего формируется застой в верхнем отделе желудка, что, в свою очередь, приводит к гипертрофии эндотелия сосудов и делает ее чувствительным к повреждающим агентам. Изучаются роль цитокинов и факторов роста, оксида азота, который вызывает гипердинамическую циркуляцию и индуцирует полнокровие и венозный застой с образованием тромбов, разрывом венул и внутрислизистыми кровоизлияниями.
В основе профилактики и лечения ПГГ лежат лечебные мероприятия, направленные на снижение давления в системе воротной вены. Наиболее часто в лечении кровотечений при ПГГ используются пропранолол, неселективные В-блокаторы, синтетический аналог соматостатина (октреотид), вазопрессин.
Портальная декомпрессия после наложения ПКШ приводит к полной регрессии патологических изменений слизистой оболочки желудка. Однако по данным литературы опыт применения TIPS для лечения портальной гипертензионной гастропатии небольшой. Процедура TIPS должна использоваться в качестве резервного метода при безуспешности других методов лечения.
Эндоскопическое лечение кровотечении при ПГГ играет малую роль, так как желудочное кровотечение имеет, как правило, диффузный характер. Аргоноплазменная коагуляция, склеротерапия, использование цианокрилатных клеевых композиций может использоваться при локальном источнике кровотечения, но на современном этапе нет надежных данных, при которых показаны надежность и эффективность эндоскопических методов гемостаза.