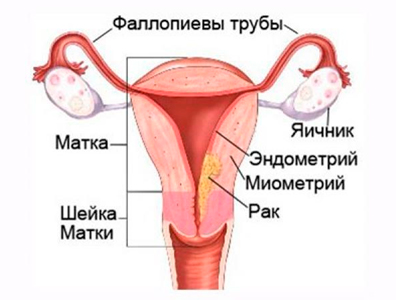
Эндометриоидная аденокарцинома с плоскоклеточной дифференцировкой что это такое
Аденокарцинома матки — симптомы, стадии, лечение, операция и прогноз
Аденокарцинома матки — опухоль злокачественного характера, берущая начало из железистых клеток эндометрия, в которых под действием различных факторов происходят патологические изменения. Аденокарцинома эндометрия матки занимает третье место среди онкологических заболеваний. У 80-90% пациенток с раком тела матки диагностируется именно аденокарцинома.
Виды аденокарцином
Эти опухоли можно разделить на два вида. К первому патогенетическому типу относятся эстрогенчувствительные опухоли, выявляемые в большинстве случаев у женщин в период менопаузы, а также у пациенток, страдающих ожирением, имеющих в анамнезе онкологические заболевания яичников, молочной железы, кишечника. Большей частью опухоли первого типа являются высокодифференцированными. Эндометриоидная аденокарцинома матки 2 типа диагностируется реже, ее особенностью является более глубокая инвазия в миометрий. Этот вид опухоли, как правило, низкодифференцированный, обладает более высокой потенцией к лимфогенному метастазированию.
Также аденокарциномы можно разделить на виды в зависимости от степени дифференцировки опухолевых клеток:
| Степень дифференцировки: | Характеристики: |
|---|---|
| высокодифференцированный рак (G 1) | встречается не более чем в 5% случаях, большинство клеток сохраняет нормальную структуру, опухоль растет медленно; |
| умеренно дифференцированный рак (G 2) | выявляется в 5-50% случаев, в структуре опухоли чаще встречаются разнородные по морфологическим признакам клетки, наблюдается усиленное деление клеток; |
| низкодифференцированный рак (G 3) | обнаруживается более чем в 50% случаев, клеточный полиморфизм выражен ярко, в структуре клеток наблюдаются множественные признаки патологических изменений; опухоль отличается быстрым и агрессивным ростом. |
Течение заболевания — стадии
Стадирование необходимо для выбора адекватной тактики лечения. Стадия аденокарциномы матки определяется на основе гистологической дифференциации и распространенности злокачественного процесса.
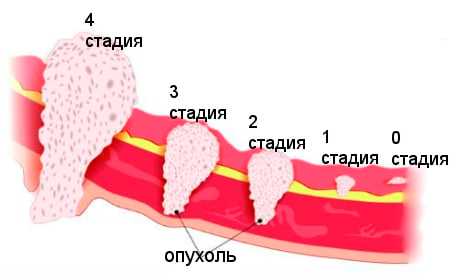
Стадии аденокарциномы матки
Определить стадию заболевания можно только в ходе обследования. Существующие сегодня методы диагностики (УЗИ, томография, гистероскопия с раздельным диагностическим выскабливанием слизистой шейки и полости матки и др.) позволяют быстро и точно определить степень развития опухоли, уровень ее дифференцировки, наличие метастазирования и др. Окончательный диагноз выставляется на основании гистологии, при аденокарциноме матки, как при любом злокачественном заболевании, гистологическое исследование частиц опухоли также служит для прогнозирования лечения.
Симптомы аденокарциномы матки
В некоторых случаях заболевание на начальных этапах протекает бессимптомно и является случайной находкой при обследовании: либо профилактическом, либо по поводу другого заболевания. Но большая часть пациенток обращается к врачу, когда появляются настораживающие признаки, при аденокарциноме матки — это кровяные выделения. У женщин, не достигших менопаузы, возникают обильные и длительные менструации, появляются выделения в межменструальный период. Также возможно появление водянистых выделений с неприятным запахом, болей тянущего характера внизу живота, отмечается диспареуния — дискомфорт и боли при половом акте. После наступления климакса характерным симптомом аденокарциномы эндометрия матки является маточное кровотечение.
На более поздних стадиях присоединяется слабость, потеря аппетита, необъяснимая потеря веса, повышение температуры. При распространении злокачественного процесса на кишку и мочевой пузырь возникают нарушения, связанные с работой этих органов. Однако эти признаки не относятся к характерным, они могут появляться и при других заболеваниях, поэтому для определения причины их появления необходимо комплексное обследование.
Лечение
Основным методом лечения аденокарциномы матки является операция, цель которой — радикальное удаление опухоли. Объем оперативного вмешательства планируется в зависимости от локализации опухоли, ее гистологической структуры, вероятности формирования регионарных метастазов и т.п.
При аденокарциноме метастазы распространяются в основном лимфогенным путем, лимфоузлы, служащие в качестве естественного барьера, на какое-то время могут задержать широкое распространение раковых клеток в другие структуры. При удалении опухоли до образования регионарных метастазов возможно стойкое излечение в большинстве случаев. При поражении регионарных лимфоузлов необходимо расширенное хирургическое вмешательство, что улучшает прогноз при аденокарциноме матки. На поздних этапах заболевания, когда пораженными оказываются отдаленные лимфоузлы, появляются метастазы в других органах, удаление первичной опухоли и регионарных лимфоузлов является частью лечения. Помимо операции, также может назначаться химиотерапия, гормонотерапия, облучение.
Хирургическое лечение
Объем оперативного вмешательства зависит от стадии болезни, которая определяется на этапе дооперационного обследования.
В нашей клинике при планировании тактики лечения у конкретного пациента принимает участие консилиум специалистов: кроме хирурга привлекаются также химиотерапевты и радиологи — независимо от предполагаемой стадии болезни.
Мой подход к лечению
Непременным условием для меня является индивидуальный подход к лечению пациентки, при этом я учитываю целый ряд деталей: возраст пациентки, наличие сопутствующих заболеваний, личные пожелания, касающиеся лечения, и др. Например, у женщин до 45 лет с диагностированной высокодифференцированной опухолью 1 стадии, при отсутствии данных об имеющихся метастазах, мутации гена BRCA или при отсутствии синдрома Линча может быть проведена экстирпация матки и удаление маточных труб с сохранением яичников. При наличии умеренно- или высокодифференцированной опухоли 1 А или 1 В стадии возможно проведение операции без тазовой и парааортальной лимфаденэктомии и т.д.
Прогноз после операции при аденокарциноме матки
Выживаемость после оперативного лечения зависит от целого ряда факторов. В первую очередь имеет значение своевременное начало терапии. Также на прогноз влияет степень дифференцировки опухоли. При высокодифференцированном раке прогноз более благоприятный, чем при низкодифференцированной опухоли. Одним из факторов прогноза является также возраст пациентки, у более молодых женщин выживаемость выше, чем у пациенток старше 70 лет.
По сводным данным Международной федерации гинекологии и акушерства, усредненные показатели пятилетней выживаемости составляют:
Хирургическое удаление аденокарциномы матки считается одним из наиболее сложных в гинекологической онкологии. Наличие в зоне операции важных для организма нервных и кровеносных структур, риск заброса частиц опухоли на здоровые ткани и т.п. — все это требует максимально бережного оперирования и огромного опыта.
За более чем 30-летний опыт работы техника операции отработана мною детально по всем этапам. Мною лично проведено более 160 лапароскопических операций у пациенток со злокачественными опухолями матки. Полученные результаты обобщены в многочисленных научных трудах и монографиях. Для гинекологов и онкологов я также ежегодно провожу мастер-классы, темой которых является хирургическое лечение рака матки.
Аденокарцинома матки
Рак тела матки – это злокачественная опухоль, под которой чаще все подразумевается рак эндометрия внутреннего слоя матки, отторгаемого во время менструации. В большинстве случаев, рак эндометрия является аденокарциномой (то есть опухолью, состоящей из железистых клеток).
Врач акушер-гинеколог высшей категории, онкогинеколог, хирург
Врач акушер-гинеколог высшей категории, оперативная гинекология
Врач акушер-гинеколог высшей категории, оперативная гинекология
Сколько лет развивается рак эндометрия?
Эндометрий – слизистая оболочка матки, создает в полости благоприятные условия для имплантации бластоцисты, но также восприимчив к любым колебаниям гормонального фона. В оболочке происходят циклические изменения в период менструального цикла. Здесь же начинается и зарождение различного вида новообразований.
Злокачественные опухоли прогрессируют в течение нескольких лет. Часто болезнь вначале протекает бессимптомно. Новообразование до поздних стадий не влияет на самочувствие женщины. Именно это является причиной того, что к нам пациентки попадают уже тогда, когда рак матки создает реальную опасность для жизни женщины. Конечно же, это плохо, но опускать руки ни в коем случае не стоит. При подборе схемы борьбы с заболеванием используется степень дифференцировки.
Аденокарцинома эндометрия G1 с высокой степенью дифференцировки. Возникает при гиперплазии эндометрия. На долю солидных участков приходится до 5%, остальные 95% – на железистые структуры.
Низкодифференцированная или солидная (G3) аденокарцинома матки. Солидные структуры превышают 50%, хотя диагностируются и железистые.
Причины и факторы риска развития рака эндометрия
Точная причина развития онкологических заболеваний на данный момент не известна, но установлено, что аденокарцинома эндометрия чаще всего развивается либо у пациенток с генетической предрасположенностью, либо при повышенном уровне эстрогена в организме женщины в течение длительного времени.
Наследственные факторы развития рака эндометрия:
Состояния, сопровождающиеся повышенным уровнем эстрогенов и повышающие шанс развития рака эндометрия:
Также повышенный риск имеют женщины, страдающие гиперплазией эндометрия.
При наличии у Вас факторов риска, особенно важно регулярно проходить профилактическое обследование у гинеколога, поскольку раннее обнаружение опухоли – основное условие для его успешного лечения.
Стадии заболевания
Прогрессируя, злокачественные гинекологические новообразования проходят нулевую и еще 4 стадии.
В Medical Plaza при стадировании рака эндометрия применяется ICG-технология, что позволяет избежать неоправданного расширения объема операции и позволяет сохранить структуры, которые при обычной операции хирургу пришлось бы удалить.
Куда метастазирует рак эндометрия?
Локализация распространения опухолевых клеток зависит от наличия инвазии болезни в миометрии и расположения рака в полости тела матки. Чаще всего метастазирование обнаруживается очагово как в одном, так и в нескольких органах – культя влагалища, брюшина, легкие, печень и кости. Проявляется в форме рецидивов и метастазов в лимфатических узлах.
Можно ли на УЗИ увидеть рак эндометрия?
На данный момент проведение гистероскопии с взятием биопсии эндометрия является золотым стандартом при диагностике гиперпластических процессов и выявлении рака эндометрия.
Для планирования объема и предварительного стадирования перед операцией проводится полное обследование в соответствии с международными онкологическими стандартами лечения онкозаболеваний:
Можно ли вылечить рак эндометрия?
Сегодня рак эндометрия матки – не приговор. При регулярных профилактических обследованиях у гинеколога и выявлении на ранних стадиях злокачественных новообразований в матке болезнь излечима. Правильное и своевременное лечение позволяет избавиться от опухоли, предотвратить ее рецидив и метастазирование. По летальности исходов данная патология занимает последнее место в списке заболеваний женских половых органов. При подборе схемы лечения аденокарциномы матки учитывается возраст пациентки, общее состояние, стадия заболевания.
При І стадии обычно требуется оперативное вмешательство для удаления матки и ее придатков. На второй стадии предполагается вместе с экстирпацией матки, придатков также аднексэктомия окружающих лимфатических узлов (возможно проникновение в них опухолевых клеток).
Обращаем внимание, что благоприятный прогноз при раке эндометрия зависти от качества хирургического этапа, что в свою очередь, в немалой степени зависит от технического оснащения операционной и квалификации операционной бригады.
Онкология эндометрия на последних стадиях требует применения лучевой и химиотерапии – проводится воздействие ионизирующей радиацией на больные клетки или терапия с помощью лекарств.
Использование нанотехнологий в лечении онкозаболеваний
Для специалистов MEDICAL PLAZA каждый пациент – это индивидуальный случай, требующий персонализированного комплексного подхода. Мы проводим лечение рака эндометрия на всех стадиях, а также работаем на предупреждение рецидива, диагностируя аномальные отклонения.
Основным этапом в лечении рака эндометрия является хирургическая операция.
Она включает в себя полное удаление матки, а также у пациентов с раком тела матки высокого риска – удаление тазовых и парааортальных лимфоузлов. Удаление всего блока лимфатических узлов, особенно вблизи крупных сосудов и нервов, всегда сопряжено с большим риском для пациентки. Однако, благодаря использованию в нашем хирургическом центре ICG-технологии, стало возможным минимизировать этот риск и избежать излишней травматизации тканей, выделив и удалив лишь несколько лимфоузлов, отвечающих за сообщение с маткой, не повреждая при этом остальные лимфоузлы и окружающие их структуры.
Химиотерапия и радиотерапия, которые назначаются на поздних стадиях – тоже важная часть лечения, но в большей мере успех зависит от хирургического этапа, а значит – от квалификации хирурга и качества хирургического оборудования.
В Medical Plaza хирургическое лечение проводится в операционной, оснащенной самым современным оборудованием от ведущих мировых производителей, а также с применением роботизированной хирургической системы DaVinci. Роботизированная хирургия позволяет максимально точно удалить опухоль при минимальной травматизации пациентки.
Преимущества такой технологии кратко можно описать так:
Как распознать рак эндометрия?
На начальных стадиях болезнь зачастую проходит бессимптомно и не замечается женщиной. Самым распространенным и, часто, единственным симптомом является появление кровянистых выделений из влагалища у женщин в постменопаузе или межменструальные кровянистые выделения у женщин репродуктивного возраста.
Появление этих симптомов не обязательно означает наличие рака в полости матки, но всегда является поводом немедленно обратиться к своему гинекологу!
Должны насторожить женщину и такие сигналы:
Сколько живут с раком эндометрия?
Болезнь коварна тем, что в ряде случаев в течение длительного периода рак может не проявляться никакими симптомами. Чем раньше обнаружена проблема, тем выше шансы пациентки на выздоровление. Наименее благоприятные прогнозы, когда наблюдаются множественные метастазы аденокарциномы матки.
Прогноз
У большинства женщин рак эндометрия обнаруживают на I или 0 стадии, выживаемость при своевременном лечении стремится к 100%. Средние показатели 5-летней выживаемости:
Стадия I и II: 75-95%
Стадия III и IV: 25-55%
При опухолях высокой степени злокачественности, опухолях с обширным распространением и у пожилых пациенток прогноз может быть хуже. И наоборот, при обнаружении рака на ранних стадиях и быстром назначении правильного лечения – шансы вылечить рак эндометрия значительно повышаются.
Залог успешного лечения заключается в раннем выявлении очага поражения органа. Поэтому при первых же тревожных симптомах немедленно запишитесь к специалисту для консультации и обследования. Своевременное обращение за профессиональной помощью в разы увеличивает благоприятный прогноз при раке эндометрия!
Эндометриоидная аденокарцинома с плоскоклеточной дифференцировкой что это такое
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России, Москва, Россия
Аденокарцинома шейки матки
Журнал: Онкология. Журнал им. П.А. Герцена. 2017;6(1): 76-80
Козаченко В. П. Аденокарцинома шейки матки. Онкология. Журнал им. П.А. Герцена. 2017;6(1):76-80.
Kozachenko V P. Adenocarcinoma of the cervix uteri. P.A. Herzen Journal of Oncology. 2017;6(1):76-80.
https://doi.org/10.17116/onkolog20176176-80
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России, Москва, Россия
В статье приводятся современные данные по эпидемиологии, этиологии, классификации, путям распространения, клинике, диагностике, дифференциальной диагностике, характеристике отдельных форм заболевания, лечению, факторам прогноза и профилактике аденокарциномы шейки матки.
ФГБУ «Российский онкологический научный центр им. Н.Н. Блохина» Минздрава России, Москва, Россия
В последние десятилетия произошло резкое увеличение частоты аденокарциномы шейки матки (АКШМ). Если в 50—60-е годы ХХ века плоскоклеточный рак шейки матки (ПКР) составлял 95% всех раковых опухолей шейки матки, то в последние десятилетия его частота снизилась до 75% за счет увеличения частоты АКШМ. Такое изменение соотношения частоты ПКР и АКШМ связано с широким внедрением метода цитологического скрининга, при котором предраковые заболевания стали значительно чаще выявляться и соответственно снижаться частота выявления ПКР. В то же время частота АКШМ стала значительно увеличиваться (до 20—25%).
Существуют сходные этиологические факторы АКШМ и ПКР в виде вируса папилломы человека (ВПЧ). Однако существуют различия в их частоте. В возникновении ПКР чаще играет роль ВПЧ 16-го типа, при АКШМ ВПЧ 16-го типа обнаруживается у 50%, а при ПКР — только у 15% больных [1, 2]. Использование оральных контрацептивов обусловливает частоту возникновения АКШМ и ПКР в равной степени [3]. Курение представляет фактор риска более существенный при возникновении ПКР и в меньшей степени — АКШМ [4]. Больше факторов риска отмечается при АКШМ, подобно таковым при раке эндометрия (ожирение, отсутствие беременности и родов) [5, 6].
Морфологическая классификация АКШМ включает в себя различные варианты аденокарциномы.
Аденокарцинома in situ
эндоцервикальная аденокарцинома, обычный тип;
серозная (папиллярная серозная);
аденокарцинома, смешанная с нейроэндокринной карциномой.
Аденокарцинома (АК) in situ — заболевание, характеризующееся наличием железистых структур, выстланных атипическим железистым эпителием с нарушением ядерно-цитоплазматического соотношения, ядер клеток, богатых хроматином. Опухолевые железы не прорастают в подлежащую ткань.
Средний возраст больных на 10—15 лет меньше, чем при инвазивной АКШМ.
Клетки опухоли содержат белок р16 и маркер Ki-67. Характерным является отсутствие рецепторов эстрогенов и прогестерона.
АКШМ обычного типа является наиболее частой формой А.К. Клетки ее содержат относительно небольшое количество муцина.
При муцинозном типе АКШМ в цитоплазме опухолевых клеток содержится слизь в виде вакуолей. Муцинозная АКШМ имеет 3 формы — желудочную, кишечную и перстневидно-клеточную. Первая форма характеризуется наличием желез желудочного типа. При второй клетки напоминают таковые карциномы толстой кишки. При третьей клетки имеют вид перстневидных, они обычно присутствуют в качестве незначительного компонента в смеси с желудочной или кишечной формой.
Ворсинчато-железистый вариант АКШМ характеризуется наличием сложных ветвящихся отростков, напоминающих тубуловорсинчатую аденому толстой кишки.
Эндометриоидная АКШМ может иметь строение эндометриоидного рака эндометрия с малым содержанием или полным отсутствием внутриклеточного муцина.
Светлоклеточная АКШМ представляет собой высокодифференцированный вариант железисто-плоскоклеточной карциномы с выраженной воспалительной инфильтрацией стромы.
Серозная АК идентична серозной АК эндометрия. Она состоит из сосочковых образований, выстланных полиморфными клетками, и диагностируется только при отсутствии рака эндометрия.
Мезонефральный вариант АКШМ возникает из мюллеровских остатков, состоит из трубчатых желез, выстланных кубическими клетками с эозинофильной цитоплазмой, в просвете желез содержится гиалин.
АК, смешанная с нейроэндокринной карциномой, характеризуется тем, что в ней содержатся клетки нейроэндокринного типа вместе с вариантами АК обычного типа.
Важное значение для клинициста с точки зрения тактики лечения имеет степень распространения опухоли.
Стадирование АК шейки матки проводится по стадиям (FIGO) и распространенности опухолевого процесса (TNM).
Пути распространения
Местное распространение АК на эндометрий происходит у 4—17% больных. АК может переходить на параметральную клетчатку, что приводит к сдавлению мочеточника. Нарушение пассажа мочи может быть также обусловлено сдавлением мочеточника увеличенными лимфатическими узлами [6—8].
При значительном распространении опухоли могут поражаться мочевой пузырь и прямая кишка [6].
Поражение лимфатических узлов происходит в обычной последовательности: парацервикальные, гипогастральные, наружные подвздошные, общие подвздошные, люмбальные и паховые. Возможно и поражение лимфатических узлов в другой последовательности. Поражение надключичных лимфатических узлов встречается редко.
Гематогенное метастазирование отмечается у 5% пациенток. При этом поражаются легкие, печень, кости, кишечник, головной мозг. Метастазы в яичниках чаще встречаются при АК, чем при ПКР (5 и 0,7% соответственно) [8—10].
Важное значение имеет обнаружение раковых клеток АК в брюшной полости, что встречается в 6,7% случаев. При этом у всех этих больных возникает рецидив заболевания [10].
Клиника
Клиническая картина при АК довольно скудна, что затрудняет раннее выявление заболевания [6]. У больных наблюдаются межменструальные кровянистые выделения различной степени. В менопаузальном периоде появляются кровянистые выделения из половых путей. При прогрессировании заболевания в малом тазу могут появиться опухолевые образования. У 50% больных отмечается эндофитный рост опухоли с диффузным распространением, в связи с чем шейка матки приобретает бочкообразную форму. Реже встречается язвенная форма, при которой поражается и экзоцервикс.
Диагностика
Диагностика АКШМ не всегда является простой задачей [6, 11]. При визуальном исследовании поверхность шейки матки может быть не изменена. Патология не всегда выявляется и при бимануальном исследовании.
При АКШМ отмечается уплотнение шейки матки, а при переходе опухоли на поверхность влагалищной части обнаруживается язва [6].
Цитологическое исследование мазков из цервикального канала также не всегда позволяет сразу установить правильный диагноз [10]. У 60% больных оно может быть неинформативным. Изменение цитологической картины с появлением эхографических признаков патологии требует углубленного исследования: гистероскопии, выскабливания цервикального канала, конусовидной биопсии шейки матки.
Определение опухолевых маркеров (РЭА, СА 125, СА 19.9) имеет значение в диагностике заболевания, при этом отмечается корреляция между уровнем маркеров и стадией заболевания.
Важное диагностическое значение для выбора тактики лечения имеют дополнительные методы исследования. В качестве обязательных процедур рекомендуется УЗИ брюшной полости, включая малый таз [6]. Необходимые данные могут быть получены и при использовании других диагностических методов. Так, МРТ органов малого таза информативна при оценке глубины инвазии опухоли и ее отношения к соседним органам и тканям и в 71—97% случаев позволяет поставить верный диагноз. При К.Т. малого таза и забрюшинного пространства можно выявить метастазы в лимфатических узлах, а при ПЭТ провести молекулярную визуализацию опухоли и ее отношение к соседним органам и тканям.
Поражение опухолевым процессом соседних органов может потребовать проведение колоноскопии или цистоскопии.
Дифференциальная диагностика
АКШМ следует дифференцировать от преинвазивной формы рака, АК эндометрия, метастатического поражения шейки. Отличительными чертами инвазивного роста АК являются инфильтративный рост, наличие реактивного состояния клеток стромы. В отличие от рака эндометрия клетки АК не содержат рецепторы эстрогенов и прогестерона. Для метастатического поражения шейки матки опухолью железистого строения характерным является отсутствие поверхностного поражения органа при наличии опухолевых элементов в просвете кровеносных и лимфатических сосудов.
Лечение
Комплекс мероприятий по лечению больных АКШМ изложен по материалам практических рекомендаций по лекарственному лечению злокачественных опухолей (Russco, 2015, с. 139—149).
Лечебные мероприятия начинаются после обязательного гистологического подтверждения диагноза. Они определяются степенью распространенности опухолевого процесса и общим состоянием пациентки.
При преинвазивной АКШМ показана экстирпация матки. Женщинам репродуктивного возраста, желающим сохранить детородную функцию, может быть произведена конизация шейки матки с последующим тщательным гистологическим исследованием.
Микроинвазивная карцинома
Критериями, которые позволяют диагностировать микроинвазивный РШМ, являются глубина инвазии и ее распространенность. Выполнения только биопсии шейки матки, как правило, бывает недостаточно. Адекватным минимальным хирургическим вмешательством, позволяющим диагностировать микроинвазию опухоли в строму шейки матки, является конизация шейки матки.
IA1 стадия (инвазия 3 мм и менее; горизонтальное распространение 7 мм и менее)
Опухолевые эмболы в лимфатических и кровеносных сосудах не меняют стадию заболевания. Адекватным объемом хирургического вмешательства при РШМ IA1 стадии является конизация шейки матки с последующим выскабливанием оставшейся части цервикального канала и по показаниям полости матки при отсутствии опухоли в краях резекции и соскобе из оставшейся части цервикального канала [12]. Если в краях резекции шейки матки или в соскобе из оставшейся части цервикального канала обнаруживаются дисплазия или клетки рака, риск остаточной опухоли достаточно высокий и, прежде чем определять дальнейшую тактику лечения, необходимо провести повторную конизацию. Это нужно для уточнения степени поражения шейки матки и определения объема последующей операции. Если при глубине инвазии опухоли в строму до 3 мм обнаруживаются раковые эмболы в кровеносных или лимфатических сосудах, возрастает риск метастатического поражения регионарных лимфатических узлов (до 15%). В этом случае больной следует выполнить модифицированную расширенную экстирпацию матки с придатками (или без придатков) (операция II типа).
IA2 стадия (инвазия более 3 и 5 мм и менее; горизонтальное распространение 7 мм и менее)
— При РШМ IA2 стадии показано выполнение модифицированной расширенной экстирпации матки (II тип).
— При противопоказаниях к хирургическому лечению может проводиться лучевая терапия (ЛТ).
— При необходимости сохранить детородную функцию у больной РШМ IA2 стадии FIGO считает возможным выполнить широкую конизацию шейки матки с экстраперитонеальной или лапароскопической тазовой лимфаденэктомией либо расширенную трахелэктомию (II тип).
IB1 и IIА1 стадии (опухоль менее 4 см)
— Показана расширенная экстирпация матки (операция III типа) или ЛТ/химиолучевая терапия по радикальной программе.
— Применение комбинации хирургического лечения с ЛТ достоверно увеличивает частоту осложнений.
— При наличии метастазов в тазовых лимфатических узлах обязательно выполнять поясничную лимфаденэктомию.
Группа высокого риска прогрессирования: при наличии одного из факторов высокого риска прогрессирования после расширенной экстирпации матки III типа (метастазы в лимфатических узлах, поражение параметриев или опухоль в краях резекции влагалища) показано проведение адъювантной химиолучевой терапии (ЛТ + еженедельное введение цисплатина в дозе 40 мг/м 2 на протяжении ЛТ).
Группа промежуточного риска прогрессирования: при отсутствии факторов высокого риска прогрессирования после расширенной экстирпации матки III типа, но при наличии как минимум двух факторов из трех (инвазия опухоли более чем на 1/3 толщины миометрия шейки матки; инвазия опухолью лимфатических и кровеносных сосудов; большой размер первичной опухоли — 4 см и более) показано проведение адъювантной ЛТ.
Группа низкого риска прогрессирования: при отсутствии факторов высокого риска прогрессирования после расширенной экстирпации матки III типа, но при наличии одного фактора из трех (инвазия опухоли более чем на 1/3 толщины миометрия шейки матки; инвазия опухолью лимфатических и кровеносных сосудов; большой размер первичной опухоли — 4 см и более) адъювантное лечение не показано.
— С целью сохранения фертильности возможно выполнение расширенной трахелэктомии (III тип).
— При невозможности проведения хирургического лечения по медицинским показаниям или по выбору пациентки возможно проведение ЛТ/химиолучевой терапии по радикальной программе.
IB2 и IIА2 стадии (опухоль более 4 см)
Возможны несколько вариантов лечения.
— Расширенная экстирпация матки (операция III типа). При наличии метастазов в тазовых лимфатических узлах обязательно выполняется поясничная лимфаденэктомия. Адъювантное лечение проводится по тем же принципам, что и при IB1 и IIА1 стадиях РШМ.
— Химиолучевое лечение (ЛТ + еженедельное введение цисплатина в дозе 40 мг/м 2 на протяжении ЛТ). Проведение адъювантной гистерэктомии после химиолучевой терапии не рекомендовано.
— Неоадъювантная химиотерапия (ХТ) с последующей расширенной экстирпацией матки III типа. Адъювантное лечение проводится по тем же принципам, что и при IB1 и IIА1 стадиях РШМ (см. выше).
IIВ—IVA стадии
— Стандартом является проведение химиолучевого лечения (ЛТ + еженедельное введение цисплатина в дозе 40 мг/м 2 на протяжении ЛТ). Перед Л.Т. при необходимости выполняется КТ/МРТ брюшной полости и малого таза, ПЭТ/КТ для оценки распространенности процесса.
— Ряд авторов допускают возможность проведения хирургического вмешательства при РШМ IIB стадии. Это позволяет избежать поздних осложнений ЛТ и химиолучевого лечения у пациенток, не имеющих факторов неблагоприятного прогноза (метастазы в лимфатических узлах, поражение параметриев и др.). У молодых пациенток можно сохранить функцию яичников и эластичность влагалища. При наличии метастазов в лимфатических узлах у молодых пациенток, производится транспозиция яичников из зоны облучения. Кроме того, удаление первичной опухоли предотвращает возникновение радиорезистентности первичной опухоли. Недостатками выполнения операции на первом этапе является риск осложнений, связанный с комбинированным или комплексным лечением пациенток.
— В случае метастатического поражения тазовых и/или поясничных лимфатических узлов возможно выполнение экстраперитонеальной лимфаденэктомии с последующим проведением химиолучевой терапии по радикальной программе. При поражении поясничных лимфатических узлов облучение проводится расширенным полем.
— Химиолучевая терапия по радикальной программе должна проводиться не более 6—7 нед, в адекватных дозах (85—90 Гр на т. А, 55—60 Гр на т. В). Увеличение продолжительности химиолучевой терапии снижает выживаемость больных.
— Роль адъювантной ХТ после химиолучевого лечения по радикальной программе не ясна. Только одно исследование указывает на значительное преимущество использования адъювантной ХТ после химиолучевого лечения по радикальной программе. Пациентки РШМ IIВ2—IV стадии получали цисплатин 40 мг/ м 2 + гемцитабин 125 мг/ м 2 еженедельно на фоне ЛТ по радикальной программе и 2 курса адъювантной ХТ после окончания ЛТ (цисплатин 50 мг/м 2 в 1-й день + гемцитабин 1000 мг/м 2 в 1-й, 8-й дни с интервалом в 3 нед). У пациенток, получавших адъювантную ХТ, отмечалось достоверное улучшение как выживаемости без прогрессирования, так и общей выживаемости.
— Эффективность проведения неоадъювантной ХТ перед операцией изучается.
— Проведение неоадъювантной ХТ с последующей ЛТ не улучшает выживаемость по сравнению с проведением только ЛТ.
— У части больных без перехода опухоли на стенку таза альтернативой химиолучевому лечению может служить экзентерация малого таза (особенно при наличии свищей). Выполнять это вмешательство можно первичным больным РШМ IVA стадии и больным с центральным рецидивом, вовлекающим мочевой пузырь и/или прямую кишку, не переходящим на стенку таза, при отсутствии диссеминации по брюшине и отдаленных метастазов. Чаще выполняется тотальная экзентерация малого таза (включающая удаление мочевого пузыря, матки, влагалища и прямой кишки). В редких случаях операция может быть ограничена передней экзентерацией (удаление мочевого пузыря, матки, влагалища) или задней экзентерацией (удаление матки, влагалища и прямой кишки).
— При наличии триады симптомов (односторонний отек нижней конечности, ишиалгия и блок мочеточника), когда в большинстве случаев диагностируется переход опухоли на стенку таза, хирургическое лечение не показано. Таким больным возможно проведение паллиативного лечения.
IVВ стадия
Для пациенток с отдаленными метастазами вариантом лечения является системная платиносодержащая химиотерапия, возможна монотерапия цисплатином (см. системная химиотерапия).