С чем уксус вступает в реакцию
С чем уксусная кислота вступает в реакцию?
Любая кислота вступает в реакцию с любой щелочью. Проще всего посмотреть на столовой соде. А вообще смотря какую реакцию нужно получить. Некоторые реакции могут проходить достаточно долго и сразу не увидишь.
Галогенами являются пять неметаллов 7 группы периодической таблицы Менделеева – фтор, хлор, бром, йод и астат. Астат сильно радиоактивен.
Химические свойства галогенов:
Молочный сахар с одной молекулой H2O. Используется в качестве подсластителя или наполнителя в таблетках, иногда в лекарственных порошках. Может использоваться в качестве нормализатора пищеварения, в том случае, если у больного нет непереносимости лактозы.
Дополню свой ответ, раз уж его прокомментировали и требуется дополнительное разъяснение.
Итак, занимаясь фотографией я усвоил один из её законов, гласящих что если с фотографии можно убрать какую то его часть и общий смысл не пострадает, то это говорит лишь о том, что фотограф не думал над композицией своей фотографии и она банально сырая. Если мысленно уберете часть изображения с марки, где расположена формула, книга, голубь и шприц с ретортой, то увидите, что Нобель как сидел так и сидит и общая композиция снимка ничуть не пострадает, так как он как смотрел на часы на стене, так и продолжает это делать с тем же успехом.
А значит, те художники, что готовили макет марки, банально заполнили её пустую часть абсолютно от балды, ничуть не заботясь о том, чтобы все это смотрелось более законченно в композиционном плане. И как я уже писал, это говорит о их «профессионализме» красноречивее всяких слов.
И чтобы стали понятны мои слова, я немного поубрал все лишнее с марки, не очень правда чистенько, но для разъяснения сути будет достаточно.
А что тут невозможного? Два атома сблизились на расстояние, достаточное для взаимодействия их электронных оболочек, а дальше произошло их слияние с образованием молекулы. Вот вам и химическая реакция. Само понятие «столкновение» относительно.
Характеристика уксусной кислоты с точки зрения практического применения.
Уксусная кислота – это вещество, которое относится к гомологическому ряду алифатических кислот. Это один из самых простых и важных членов этого ряда, поэтому физико-химическая характеристика уксусной кислоты будет более чем необходима.
Если рассматривать кислоту в чистом виде, то это бесцветная жидкость, поглощающая влагу из воздуха. Плотность уксусной кислоты составляет 1,04723 г/см3. При охлаждении вещества до 16,63°С образуется ледяная уксусная кислота в виде кристаллов.
То касается химических характеристик, то уксусная кислота относится к одноосновным кислотам. Химический характер вещества определяется наличием карбоксила СООН. Она является достаточно слабой кислотой, поскольку ее константа электролитической диссоциации равняется 1,82*10-5 моль/л при температуре 18°С. Она способна с легкостью нейтрализовать ключевые окиси, их гидраты, а также вытеснять из углекислых солей углекислоту.
Химические характеристики уксусной кислоты на примерах.
Ацетаты щелочных металлов, а также некоторых других (меди, олова, свинца, одновалентной ртути) растворимы также в спирте, однако количество растворяющейся соли зависит от числа молекул кристаллизационной воды в соли или от содержания влаги в спирте. Соли, не содержащие кристаллизационной воды (даже литиевая), не растворяются в абсолютном спирте, а также в ацетоне. Растворимость этих солей в воде при добавлении спирта или ацетона понижается, поэтому из водного раствора соли выпадают в осадок.
Если же взять водный насыщенный раствор уксуснокислого кальция (1 часть) и быстро влить в сосуд, содержащий этиловый спирт (1,7 части), то вся жидкость тотчас затвердевает. Получаемый подобным путем «сухой спирт» при поджигании медленно сгорает не коптящим пламенем, оставляя углекислый кальций. Такое «топливо» особенно удобно для туристов.
Уксуснокислые соли олова и свинца (металлов подгруппы германия), хорошо растворимые в воде, дают бесцветные малодиссоциированные растворы.
Взаимодействие уксусной кислоты с солями.
Уксуснокислые соли очень слабы оснований (железа, алюминия, хрома) в случае выпаривания или кипячения раствора полностью разлагаются на снование и кислоту. Очень сильные минеральные кислоты (соляная, серная и другие), а также органические нелетучие кислоты (винная, щавелевая) вытесняют кислоту из ее солей.
Муравьиная кислота тоже способна вытеснять уксусную кислоту из ее солей. Но эта реакция не способна дойти до конца даже в случае переизбытка муравьиной кислоты. Чистая уксусная кислота способна образовать основные соли: причем если щелочноземельные и щелочные металлы дают только соли среднего типа, то тяжелые металлы способны давать основные соли. Соли уксусной кислоты основной группы получаются в случае действия на гидраты или окиси окисей растворов средних солей уксусной кислоты.
Из данных солей основной уксуснокислый свинец используется в технике для изготовления свинцовых белил, а в медицине в качестве свинцовой примочки. Основная уксуснокислая медь, которая называется «ярь-медянка» используется как зеленая краска, а в сочетании с мышьяковистокислой медью входит в состав очень ядовитой швейнфуртской, или парижской зелени.
Карбоновые кислоты
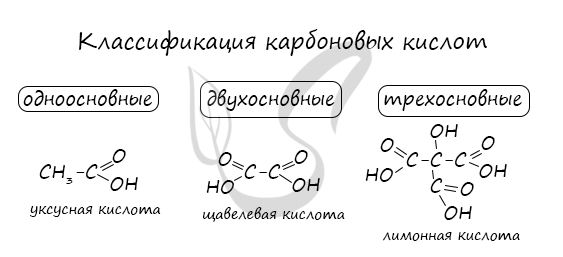
Классификация карбоновых кислот
Высшие карбоновые кислоты называют жирными кислотами. Более подробно мы изучим их теме, посвященной жирам, в состав которых они входят.
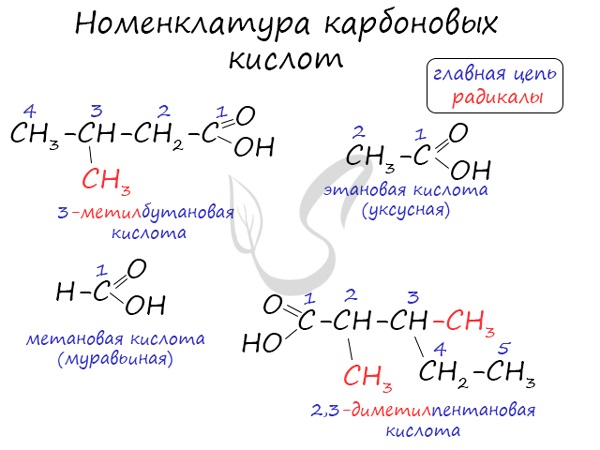
Номенклатура и изомерия карбоновых кислот
Названия карбоновых кислот формируются путем добавления суффикса «овая» к названию алкана с соответствующим числом атомов углерода и слова кислота: метановая кислота, этановая кислота, пропановая кислота, и т.д.
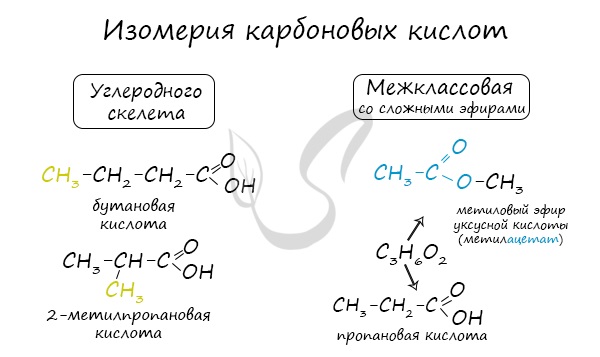
Для предельных карбоновых кислот характерна структурная изомерия: углеродного скелета, межклассовая изомерия со сложными эфирами.
Получение карбоновых кислот
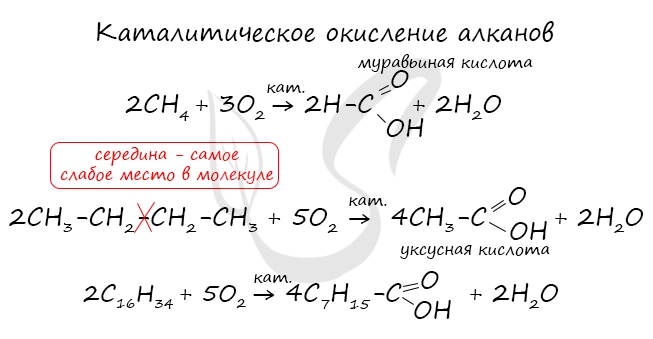
При повышенной температуре и в присутствии катализатора становится возможным неполное окисление алканов, в результате которого образуются кислоты.
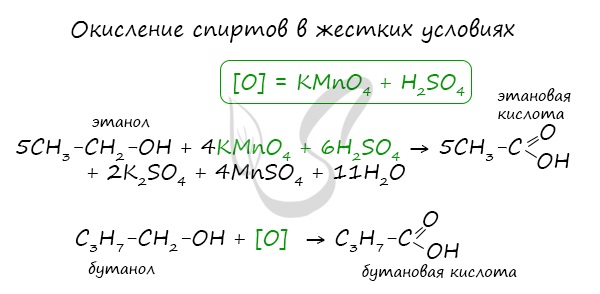
При реакции спиртов с сильными окислителями, такими как подкисленный раствор перманганата калия, спирты окисляются до соответствующих кислот.
Обратите особое внимание, что при написании реакции с аммиачным раствором серебра в полном виде, правильнее будет указать не кислоту, а ее аммиачную соль. Это связано с тем, что выделяющийся аммиак, который обладает основными свойствами, реагирует с кислотой с образованием соли.
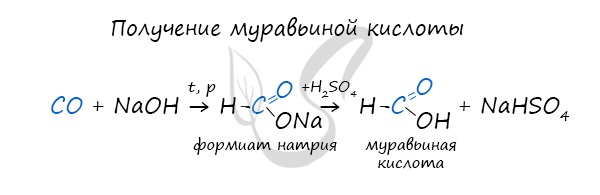
При дальнейшей обработке формиата серной кислотой образуется муравьиная кислота.
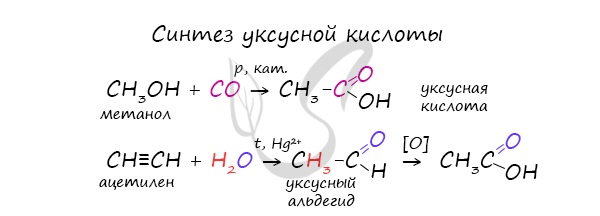
Специфичность синтеза уксусной кислоты заключается в реакции угарного газа с метанолом, в результате которой она образуется.
Также уксусную кислоту можно получить другим путем: сначала провести реакцию Кучерова, в ходе которой образуется уксусный альдегид. Окислить его до уксусной кислоты можно аммиачным раствором оксида серебра или гидроксидом меди II.
Химические свойства карбоновых кислот
Для карбоновых кислот не характерны реакции присоединения. Карбоновые кислоты обладают более выраженными кислотными свойствами, чем спирты.
Карбоновые кислоты вступают в реакции с металлами, которые способны вытеснить водород (стоят левее водорода в ряду напряжений металлов) из кислоты. Реагируют также с основаниями, с солями более слабых кислот, например, угольной кислоты.
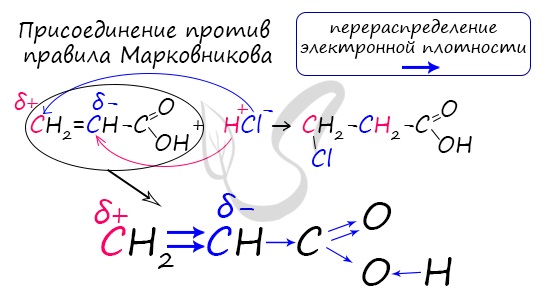
Перераспределение электронной плотности в молекулах этих кислот для лучшего запоминания лучше увидеть наглядно. Это перераспределение обусловлено большей электроотрицательностью хлора, который притягивает электронную плотность.
Муравьиная кислота отличается от своих гомологов. За счет наличия у нее альдегидной группы, она, единственная из карбоновых кислот, способна вступать в реакцию серебряного зеркала.
В такой реакции идет ее окисление до нестойкой угольной кислоты, которая распадается на углекислый газ и воду.
При нагревании и в присутствии серной кислоты (водоотнимающего компонента) муравьиная кислота распадается на воду и угарный газ.
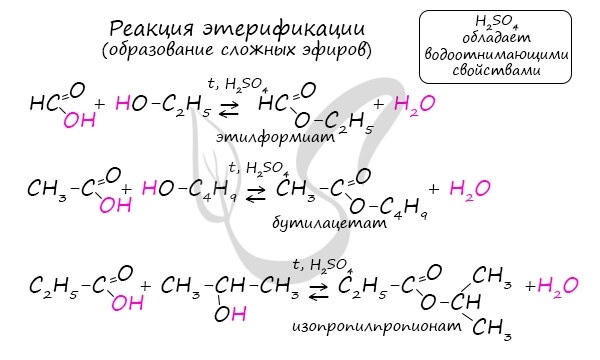
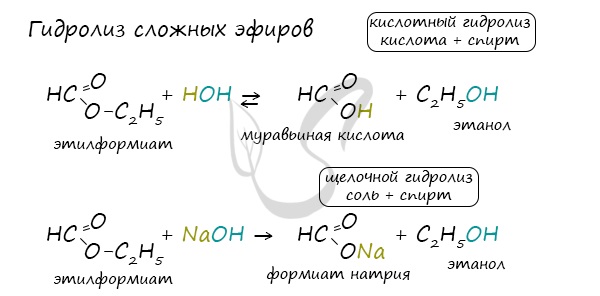
Сложные эфиры
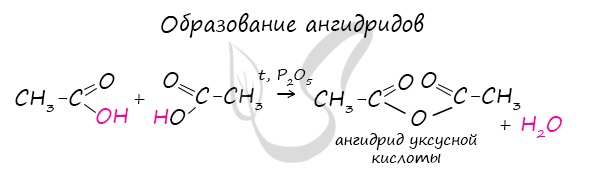
Ангидриды
Хлорангидриды карбоновых кислот образуются в реакции карбоновых кислот с хлоридом фосфора V.
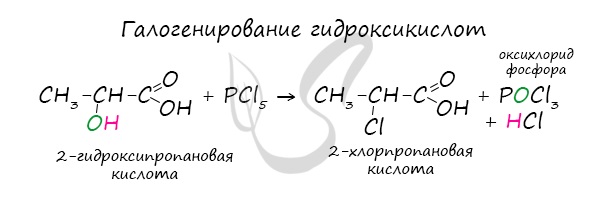
Следующая реакция не имеет отношения к ангидридам, однако (из-за их схожести) вы увидите ее здесь для наилучшего запоминания. Это реакция галогенирования гидроксикислот, в результате которой гидроксогруппа в радикале меняется на атом галогена.
Непредельные карбоновые кислоты
Распределение электронной плотности в молекулах творит чудеса: иногда реакции идут против правила Марковникова. Так происходит в непредельной акриловой кислоте.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Характеристика и свойства уксусной кислоты
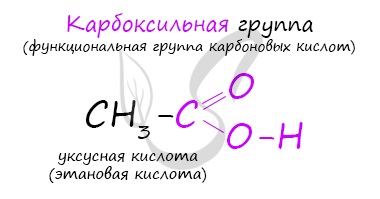
Уксусная кислота (или этановая) – органическое химическое соединение, относящееся к карбоновым кислотам (в состав их формулы входит карбоксильная группа – COOH). Это вещество известно человечеству с древних времен. Без нее невозможно производство многих пищевых продуктов и получение органических веществ.
Общая характеристика, формула
Химическая формула вещества СН3СООН. При нормальных условиях это бесцветная жидкость, обладающая резким характерным запахом и кислым вкусом. Попадание концентрированного вещества на слизистые оболочки вызывает химический ожог. «Ледяная» уксусная кислота 99 процентов обладает высокой гигроскопичностью, т.е. она способна поглощать водяной пар из атмосферного воздуха.
В уксусе могут растворяться не только жидкости, но и газы. Например, в нем растворяются фтороводород HF, хлористый водород HCl и бромистый водород HBr.
Соли рассматриваемого химического вещества называются ацетатами. Такое же наименование имеют и сложные эфиры. В качестве пищевой добавки применяется раствор уксусной кислоты с концентрацией 3 – 9%. В составе уксусной кислоты не может быть никаких примесей.
История открытия уксусной кислоты
Рассматриваемое вещество известно человеку с первобытных времен. СН3СООН образуется при скисании вина (отсюда и другое название – винный уксус). Впервые химические свойства уксуса описано в Древней Греции в 3 веке до н.э. В то время это вещество применялось для получения красителей. В Древнем Риме большой популярностью пользовался так называемый свинцовый сахар – ацетат свинца. Эта соль была причиной хронических отравлений и болезней римской аристократии.
Химическое строение уксуса впервые начал исследовать французский химик Дюма: он опубликовал труд о замещении атома водорода в органических соединениях атомом хлора. Так он получил хлоруксусную кислоту.
В середине 19 века немецкий химик А. Кольбе синтезировал уксус путем хлорирования сероуглерода CS2 до тетрахлометана CCl4, который путем пиролиза превращался в тетрахлорэтилен C2Cl4. Дальнейшее воздействие хлором водного раствора тетрахлорэтилена дало возможность получить трихлоруксусную кислоту. После электролитического восстановления ученый получил СН3СООН.
Еще в начале ХХ века значительное количество уксуса проводилось путем перегонки древесины.
Получение и производство
На ранних этапах развития индустрии вещество уксусная кислота получали путем окисления бутана и ацетатальдегида. Этот альдегид окислялся в присутствии катализатора ацетата марганца при высоком давлении и температуре. Реакция имела такой вид: 2СН3СНО + О2→2СН3СООН.
Окисление же бутана проходило при высоком давлении и в присутствии катализатора ацетата кобальта. Реакция имела такой вид: 2С4Н10 + 5О2→ 2СН3СООН.
В результате подорожания нефти (а рассмотренные способы базировались на окислении продуктов ее крекинга) сделали такие химические реакции экономически невыгодными. Более совершенный способ получения уксусной кислоты – это каталитическое карбонилирование метанола (древесного спирта) путем воздействия на него окисью углерода. Реакция имеет такой вид: СН3СОН + СО → СН3СООН. Катализатором служит йодистая соль кобальта.
С 1970 г. компания Монсанто предложила использовать в качестве катализатора родиевые соли. В результате производство уксусной кислоты заметно возросло.
В процессе биохимического производства применяется окисление этилового спирта микроорганизмами. Реакция проходит при участии фермента алькогольдегидрогеназы.
Также пищевую добавку уксусную кислоту можно получить путем окисления этилового спирта: С2Н5ОН + О2→ СН3СООН + Н2О.
Химические и физические свойства
Физические свойства уксусной кислоты следующие:
В следующих примерах показаны кислотные свойства уксусной кислоты.
Качественной реакцией на наличие ацетатов является их взаимодействие с сильными кислотами. Уксус вытесняется из водных растворов солей. При этом появляется характерный запах.
Хранение и транспортировка
Промышленная уксусная кислота наливается в транспортную тару (оцинкованные металлические бочки или канистры из полимерных материалов). В магазины раствор поступает в стеклянных или пластиковых бутылках с навинчивающимися крышками или пробками.
Хранить это вещество нужно в плотно закрытой таре в помещениях, которые специально приспособленные для хранения воспламеняющихся веществ. Места хранения уксусной кислоты должны быть защищенными от попадания прямых солнечных лучей и осадков.
Класс опасности уксусной кислоты – 8: едкие и коррозийные вещества.
Перевозку нужно осуществлять в цистернах из нержавеющей стали. Они не должны иметь нижнего слива. Наливные отверстия, люки оборудуются герметичными резиновыми, полиэтиленовыми прокладками, которые предотвращают расплескивание жидкости в процессе перевозки.
ООО «Эверест» осуществляет оптовые поставки уксусной ледяной (этановой) кислоты по выгодным ценам. Подробнее по телефону: +7 (812) 448-47-55.
Уксусная кислота. Химико-токсикологический анализ
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Уксусная кислота. Химико-токсикологический анализ
Уксусная кислота (этановая кислота) СН3СООН – бесцветная прозрачная жидкость с резким запахом. Для безводной («ледяной») т.пл. 16,64 °С, т. кип. 117,8 °С. Смешивается со многими растворителями, хорошо растворяет органические соединения.
Уксусная кислота – один из главных промежуточных метаболитов, выполняющих как структурную, так и энергетическую функцию в обмене веществ.
Пары уксусной кислоты раздражают слизистые оболочки верхних дыхательных путей, растворы (концентрация выше 30 % по массе) при соприкосновении с кожей вызывают ожоги.
Уксусная кислота используется в пищевой, химической промышленности, в фармации.
Химико-токсикологическое исследование на наличие уксусной кислоты проводят при специальных заданиях или при наличии соответствующих указаний в материалах делах.
Уксусная кислота. Изолирование.
Уксусную кислоту отгоняют из объектов биологического происхождения, подкисленных 10 % кислоты серной или фосфорной. Дистиллят собирают в сосуд, содержащий 0,1 моль/л раствор натрия гидроксида, ввиду летучести уксусной кислоты. Количество уксусной кислоты определяют оттитровывая кислотой избыток натрия гидроксида.
Уксусная кислота. Качественное обнаружение
1. Реакция с хлоридом железа (III)
Появляется красная окраска. При нагревании окрашенного раствора происходит гидролиз, в результате которого выпадает бурый осадок.
Чувствительность реакции 1,25 мг.
2. Реакция этерификации (образования этилацетата) реакция протекает при нагревании с серной кислотой.
Появляется специфический запах этилацетата.
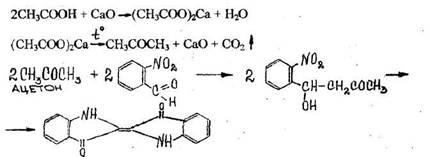
3. Реакция образования индиго
При нагревании уксусной кислоты с солями кальция образуется ацетон, который подвергается конденсации с о-нитробензальдегидом.
Чувствительность реакции 10 мг.